题目内容
(9分)铝、铁、铜是我们生活中常见的金属。
(1)铝制品具有很好的耐腐蚀性能,原因是 。
(2)铁生锈的条件是 ,生活中防止铁生锈的方法有
(写一种即可)。
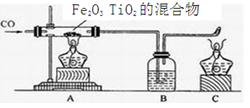
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是 (用化学方程式表示)。
(4)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如图所示:
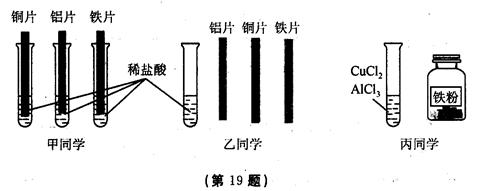
①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu。
②乙同学只用一支试管,取一次稀盐酸也能证明Al>Fe>Cu。他在稀盐酸中插入金属的顺序为: 或 ,写出其中一个反应的化学方程式 。
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是 。
(1)铝制品具有很好的耐腐蚀性能,原因是 。
(2)铁生锈的条件是 ,生活中防止铁生锈的方法有
(写一种即可)。
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是 (用化学方程式表示)。
(4)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如图所示:

①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu。
②乙同学只用一支试管,取一次稀盐酸也能证明Al>Fe>Cu。他在稀盐酸中插入金属的顺序为: 或 ,写出其中一个反应的化学方程式 。
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是 。
(1)铝易与氧气反应,在其表面形成一层致密的氧化铝薄膜,阻止铝进一步被氧化
 (2)与氧气和水(或水蒸气)接触 涂油(或镀其他金属、刷漆等其他防锈方法)
(2)与氧气和水(或水蒸气)接触 涂油(或镀其他金属、刷漆等其他防锈方法)
(3)Fe203+3C0 2Fe+3CO2
(4)①铝片表面比铁片表面产生气泡快(或铝片和铁片表面都有气泡产生,且铝比铁反应剧烈)
②Fe、Cu、Al(或Cu.Fe、Al)(名称也可) Cu、Fe、Al(或Fe、Cu、Al)(名称也可) Fe+2HCl=FeCl2+H2↑(或3FeCl2+2A1=2AlCl3+3Fe)
③FeCl2、AlCl3(或氯化亚铁、氯化铝)
 (2)与氧气和水(或水蒸气)接触 涂油(或镀其他金属、刷漆等其他防锈方法)
(2)与氧气和水(或水蒸气)接触 涂油(或镀其他金属、刷漆等其他防锈方法)(3)Fe203+3C0 2Fe+3CO2
(4)①铝片表面比铁片表面产生气泡快(或铝片和铁片表面都有气泡产生,且铝比铁反应剧烈)
②Fe、Cu、Al(或Cu.Fe、Al)(名称也可) Cu、Fe、Al(或Fe、Cu、Al)(名称也可) Fe+2HCl=FeCl2+H2↑(或3FeCl2+2A1=2AlCl3+3Fe)
③FeCl2、AlCl3(或氯化亚铁、氯化铝)
(1)铝制品具有很好的耐腐蚀性能,原因是铝易与氧气反应,在其表面形成一层致密的氧化铝薄膜,阻止铝进一步被氧化。
(2)铁在空气中生锈的条件是与氧气和水(或水蒸气)接触;生活中防止铁生锈的原理是隔绝水或氧气或形成合金等,具体的方法有涂油(或镀其他金属、刷漆等其他防锈方法)
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是:用一氧化碳还原氧化铁,生成铁和二氧化碳,反应为:Fe203+3C0 = 2Fe+3CO2
(4) 三种金属的活动性顺序为Al>Fe>Cu,即排在前面的金属能将后面的金属从其盐溶液中置换出来,判断金属的活动性。答案为Fe、Cu、Al(或Cu.Fe、Al) ;Fe+2HCl=FeCl2+H2↑(或3FeCl2+2A1=2AlCl3+3Fe);铁粉放入CuCl2和AlCl3的混合溶液中,铁能置换出铜,但不能置换出铝,因此滤液中一定会有AlCl3,因为铁粉放入CuCl2中会生成FeCl2,因此滤液中一定也含有FeCl2,固体中加入稀盐酸,无明显现象,可能CuCl2与铁恰好完全反应,也可能有剩余,不能确定CuCl2是否一定存在,故答案为FeCl2、AlCl3(或氯化亚铁、氯化铝)
(2)铁在空气中生锈的条件是与氧气和水(或水蒸气)接触;生活中防止铁生锈的原理是隔绝水或氧气或形成合金等,具体的方法有涂油(或镀其他金属、刷漆等其他防锈方法)
(3)高炉中以赤铁矿(主要成分氧化铁)为原料炼铁的原理是:用一氧化碳还原氧化铁,生成铁和二氧化碳,反应为:Fe203+3C0 = 2Fe+3CO2
(4) 三种金属的活动性顺序为Al>Fe>Cu,即排在前面的金属能将后面的金属从其盐溶液中置换出来,判断金属的活动性。答案为Fe、Cu、Al(或Cu.Fe、Al) ;Fe+2HCl=FeCl2+H2↑(或3FeCl2+2A1=2AlCl3+3Fe);铁粉放入CuCl2和AlCl3的混合溶液中,铁能置换出铜,但不能置换出铝,因此滤液中一定会有AlCl3,因为铁粉放入CuCl2中会生成FeCl2,因此滤液中一定也含有FeCl2,固体中加入稀盐酸,无明显现象,可能CuCl2与铁恰好完全反应,也可能有剩余,不能确定CuCl2是否一定存在,故答案为FeCl2、AlCl3(或氯化亚铁、氯化铝)

练习册系列答案
相关题目