题目内容
【题目】松花皮蛋是我们喜爱的食品。某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等。同学们对料泥进行了如下探究:
【猜想】猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、Ca CO3、灰份;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰份。
【实验与现象】实验过程与现象如下图:
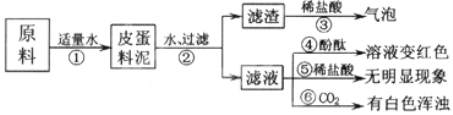
【问题与讨论】
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、_________,玻璃棒在步骤②中的作用是_______________________。
(2)步骤③的现象说明滤渣中含有:_________________________________(写化学式)。
(3)请写出步骤①发生的任意两个反应的化学方程式:___________________、________________________________。
(4)由上述实验现象推断,猜想______________________是正确的。
【答案】 漏斗 引流 CaCO3 CaO+H2O═Ca(OH)2 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH(三个化学方程式任意写两个即可) Ⅰ
【解析】(1)、过滤需要使用的仪器有:铁架台、漏斗、烧杯和玻璃棒;为防止液体倾倒时冲破滤纸,应使液体沿玻璃棒引入;(2)、滤渣加盐酸产生气体,固体物质可能是金属单质或碳酸盐;碳酸盐与盐酸反应,放出气体二氧化碳;(3)、生石灰为氧化钙的俗称,遇水生成氢氧化钙;氢氧化钙可与原料中的纯碱或草木炭发生反应生成碳酸钙沉淀和氢氧化钠、氢氧化钾;(4)、猜想II中的碳酸钠不发生反应残留在滤液中,当向滤液中滴加稀盐酸时会产生二氧化碳气体;若向猜想II的滤液中通入二氧化碳,氢氧化钠、氢氧化钾与二氧化碳反应不会出现沉淀。解:(1)、步骤②需要进行过滤,过滤需要选择的玻璃仪器有漏斗、烧杯和玻璃棒;其中玻璃棒用于液体的引流,防止直接倾倒冲破滤纸;(2)、步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有CaCO3沉淀;(3)、原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾。故反应的化学方程式为:CaO+H2O═Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH或K2CO3+Ca(OH)2=CaCO3↓+2KOH;(4)、步骤⑤向滤液中滴加盐酸无气体产生,可说明滤液中不含量碳酸盐,而猜想II中的碳酸钠没有发生反应残留在滤液中,与实验现象不符;向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,与猜想二不符。故猜想II不正确,猜想Ⅰ正确。