��Ŀ����
����Ŀ�����ᣨH2SO4����һ�ֳ��õĻ�ѧ�Լ���
��1��������_______��Ԫ����ɣ�0.1mol���������Ϊ____________g��Լ��_________����ԭ�ӡ�
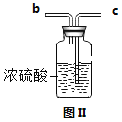
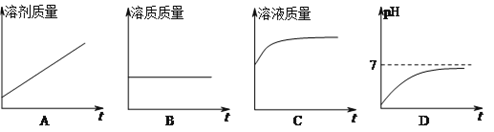
��2����Ũ���᳨�ڷ��ڿ����У�Ũ�����и�������ʱ��ı仯��ϵͼ��ȷ����________��
��3����98%��Ũ����10g���Ƴ�10%��ϡ���ᣬ���ˮ________mL��
��4����һ�������������������ϡ����������ȫ��Ӧ���۲쵽������____________________��д����ʵ������з�������һ����ѧ����ʽ_______________��
��5��ϡ�����ϡ����������ƵĻ�ѧ���ʣ����������������ѡ�õĻ�ѧ�Լ���______��
���𰸡� 3 9.8 2.408��1023 BC 88 ������ʧ����Һ���ɫ�������ݲ��� Fe2O3+3H2SO4![]() Fe2(SO4)3+3H2O��Fe+H2SO4
Fe2(SO4)3+3H2O��Fe+H2SO4![]() FeSO4+H2�� BaCl2 /Ba(NO3)2 /Ba(OH)2��Һ
FeSO4+H2�� BaCl2 /Ba(NO3)2 /Ba(OH)2��Һ
��������������Ҫ����������ʡ���1������Ļ�ѧʽΪH2SO4�������⡢����������Ԫ�أ���1mol���������Ϊ98g����0.1mol���������Ϊ9.8g��1����������к���4����ԭ�ӣ�����0.1molԼ��2.408��1023����ԭ�ӡ�
��2��Ũ��������ˮ�ԣ���Ũ���᳨�ڷ��ڿ����У�Ũ������ˮ���ӣ�������Һ���������ӣ������������٣���ѡ��BC��ϡ����Һʱ�����ʲ��䣬��ϡ�ͺ���Һ������ΪX��98%*10g==X*10% X=98g 98g��10g==88g.
����������ijɷ�Ϊ����������ϡ���ᷴӦ������������ˮ������������ɫΪ��ɫ����������Ӧ����������������Ӧ�������������������������ԣ��۲쵽������������ʧ����Һ���ɫ�������ݲ�������ѧ����ʽΪFe2O3+3H2SO4===Fe2(SO4)3+3H2O
��5��ϡ�����ϡ���ᶼ���ᣬ�������ƵĻ�ѧ���ʣ����Ը���������������������ᱵ��Ӧ���ɰ�ɫ��������������������Ӧ���ɰ�ɫ���������Դ�Ϊ��Ba(NO3)2��Һ

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�