题目内容
【题目】CO2 可用于制备碳酸饮料,人饮后有清凉感。某同学设计如下实验,测定某品牌碳酸饮料中的CO2 的含量。
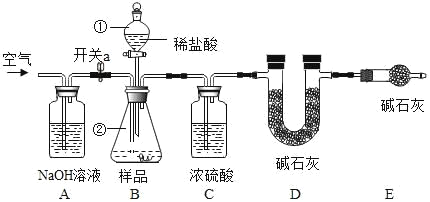
实验步骤:
①将 250mL 瓶装碳酸饮料放在冰箱中冷冻至刚好结冰;
②将饮料从冰箱内取出,迅速加入质量分数为 50%NaOH 溶液 5mL;倒转饮料瓶,轻轻震荡,完全反应,然后放置恢复至室温,待测定;
③称得装置 D 的质量为 x g,按上图连接实验装置。将步骤②中待测液全部加入仪器②中,关闭开关 a, 打开仪器①的活塞,向仪器②中注入稀盐酸,至不再产生气泡,关闭仪器①的活塞;
④打开开关 a,向装置中鼓入空气,一段时间后,称量 D 装置质量为 y g。
注:实验中各种溶液的密度都视为 1g/mL。碱石灰是 CaO 与 NaOH 的固体混合物。
(1)步骤②中发生反应的化学方程式为___________。
(2)E 装置的作用是_________。
(3)根据题中提供的数据计算此品牌碳酸饮料中 CO2 的含量为_____________g/L。
(4)步骤④鼓入空气的目的是___________。
(5)若没有 C 装置,则测得 CO2 含量会_____________(填“偏大”“偏小”“无法确定”)。
【答案】2NaOH+CO2=Na2CO3+H2O; 防止空气中的二氧化碳和水进入D装置,影响实验准确性; ![]() 让生成的二氧化碳全部进入装置C中; 偏大
让生成的二氧化碳全部进入装置C中; 偏大
【解析】
(1)加入质量分数为 50%NaOH 溶液是为了吸收二氧化碳,氢氧化钠与二氧化碳生成碳酸钠和水,发生的化学方程式为:
2NaOH+CO2=Na2CO3+H2O,故填:2NaOH+CO2=Na2CO3+H2O;
(2)E 装置的作用是吸收空气中的二氧化碳和水,防止空气中的二氧化碳和水进入D装置,影响实验准确性;
(3)碳酸饮料中的二氧化碳通过步骤②被固定(加入氢氧化钠二氧化碳会和氢氧化钠会生成碳酸钠和水),转移到B中碳酸钠和稀盐酸反应再次生成二氧化碳,D装置碱石灰能吸收二氧化碳,最终被D装置吸收,故D 装置增加的质量就是碳酸饮料中二氧化碳的质量,D 装置增加的质量为yg-xg,故此品牌饮料中CO2 的含量为![]() 故填:
故填:![]()
(4)鼓入空气的目的是让生成的二氧化碳全部进入装置C中,故填:让生成的二氧化碳全部进入装置C中;
(5)没有装置C水蒸气会进入D,使得测量二氧化碳含量偏大,故填:偏大

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】(4分)KNO3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
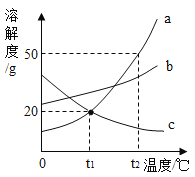
(1)依据上表数据,绘制KNO3和KCl的溶解度曲线,右图中能表示KNO3溶解度曲线的是 。(填m或n)
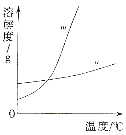
(2)由表中数据分析可知, KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是 。
(3)10℃时,131g 饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为 。
(4)如右图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的________(填字母序号)。
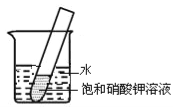
A.氢氧化钠固体 B.生石灰固体
C.冰块 D.硝酸铵固体
E.浓硫酸
【题目】KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度 | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
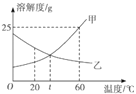
(1)由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是______.
(2)10℃时,131g饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为______.
(3)如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的______(填字母序号).
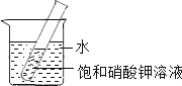
a.氢氧化钠固体 b.生石灰固体 c.硝酸铵固体