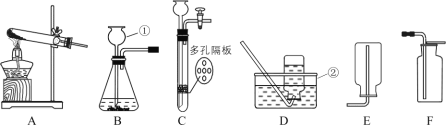
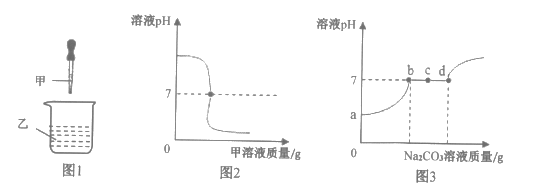
题目内容
【题目】同学们用氢氧化钠溶液和氢氧化钡溶液和无色酚酞溶液进行碱与指示剂作用的分组实验,实验结束后所有废液都倒入到同一废液缸中,为了使废液实现无害化排放,同学们向其中加入适量稀硫酸至溶液恰好变为无色,共用去质量分数为19.6%的稀硫酸200g,同学们将混合物过滤,得到白色沉淀23.3g,向滤液中加入23.3g水,得到600g7.1%的只含一种溶质的溶液,根据以上信息回答下列问题
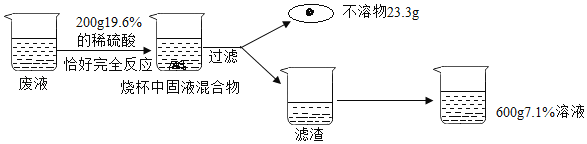
(1)写出产生白色沉淀的化学方程式_____;
(2)求解混合物中氢氧化钠的质量(x)的比例式_____;
(3)请用具体数据写明滴加稀硫酸的整个过程中,烧杯中各溶质的质量变化为_____;
(4)若实验中所用氢氧化钡溶液的浓度为17.1%,则氢氧化钠溶液的浓度为_____(酚酞溶液的体积忽略不计);
(5)若用质量分数为98%的浓硫酸配制上述实验所用的稀硫酸,需加水的质量为_____。
【答案】Ba(OH)2+H2SO4=BaSO4↓+2H2O ![]() 氢氧化钡的质量由17.1g变成0g,氢氧化钠的质量由24g变成0g;硫酸钠的质量由0g变成42.6g 6% 160g
氢氧化钡的质量由17.1g变成0g,氢氧化钠的质量由24g变成0g;硫酸钠的质量由0g变成42.6g 6% 160g
【解析】
(1)氢氧化钡与硫酸反应生成硫酸钡白色沉淀和水,化学方程式为:Ba(OH)2+H2SO4=BaSO4↓+2H2O;
(2)解:设生成23.3g硫酸钡沉淀需要硫酸的质量为m,需要氢氧化钡的质量为n。
 ;
;
![]()
m=9.8g
![]()
n=17.1g
则与氢氧化钠反应的硫酸的质量为:200g×19.6%﹣9.8g=29.4g
设与29.4g硫酸反应所需要氢氧化钠的质量为x,生成硫酸钠的质量为y,则:

![]()
x=24g
![]()
y=42.6g
(3)根据计算数据可知,滴加稀硫酸的整个过程中,烧杯中氢氧化钡的质量由17.1g变成0g,氢氧化钠的质量由24g变成0g;硫酸钠的质量由0g变成42.6g;
(4)设废液的质量为w,由质量守恒定律可知:w+200g=600g, w=400g
则氢氧化钠溶液的浓度为![]() ;
;
(5)若用质量分数为98%的浓硫酸配制上述实验所用的稀硫酸,根据稀释前后溶质质量不变计算。
设需要加水的质量为s,则: 200g×19.6%=(200g﹣s)×98%
s=160g

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案