题目内容
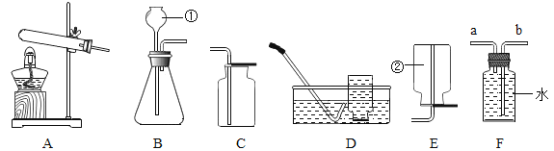
【题目】(一)下图是实验室制取气体的发生装置和气体收集装置。
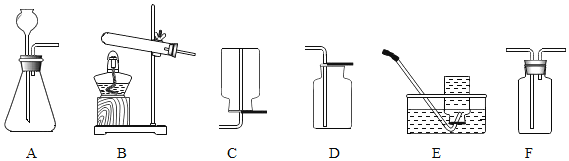
回答下列问题:
(1)用装置A和E制取氧气,其反应的化学方程式是_____________________。
(2)现需要制取并收集一瓶氢气,在装置A、B、C、D、E中,应选择的装置组合是_________。
(3)C、D、E、F都是实验室制取气体的收集装置,其中装置C和装置E不能用来收集二氧化碳,原因是_______________________。
(4)F装置可以作为多功能瓶,如果想除去制取二氧化碳中混有的氯化氢气体,瓶中应盛放_________,气体从______通入(填“左”或“右”);如果想用此瓶收集氨气,气体应从______通入(填“左”或“右”)。
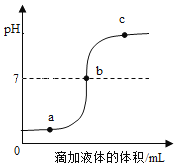
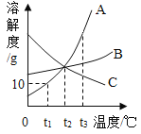
(二)生活中经常遇到一些“长相”类似的物质,如家庭制作食品用到的碳酸钠和碳酸氢钠。区分二者,比较简单的方法就是溶解度法(溶解度曲线见下图)。
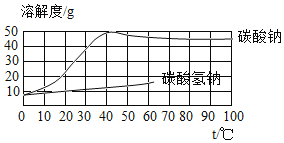
①小亮同学利用这种方法,在室温条件下设计了下面实验,请完善实验内容:
实验步骤 | 现象和结论 |
取两只试管,各倒入10g水,分别向两试管中逐步加入碳酸钠和碳酸氢钠固体,充分振荡、静置、观察现象。 | 至固体不能再溶解为止,其中,固体溶解量少的,所对应的物质是 ________(填化学式,下同),另一种物质是_________。 |
②现有碳酸钠(2g)、碳酸氢钠(2g)和足量蒸馏水。请仿照上述①中的方法和实验设计,在室温条件下,调整变量、自主设计实验,进一步区分碳酸钠、碳酸氢钠两种物质:
实验步骤 | 现象和结论 |
_________________ | ____________________ |
【答案】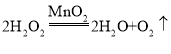 AC或AE 二氧化碳溶于水,密度比空气大 饱和碳酸氢钠溶液 左 右 NaHCO3 Na2CO3 取两只试管,分别加入2g碳酸钠和2g碳酸氢钠,分别向两试管中逐步加入蒸馏水,充分振荡、静置、观察现象 至固体完全溶解,其中,消耗蒸馏水多的,所对应的物质是碳酸氢钠,消耗蒸馏水少的,所对应的物质是碳酸钠
AC或AE 二氧化碳溶于水,密度比空气大 饱和碳酸氢钠溶液 左 右 NaHCO3 Na2CO3 取两只试管,分别加入2g碳酸钠和2g碳酸氢钠,分别向两试管中逐步加入蒸馏水,充分振荡、静置、观察现象 至固体完全溶解,其中,消耗蒸馏水多的,所对应的物质是碳酸氢钠,消耗蒸馏水少的,所对应的物质是碳酸钠
【解析】
(一)(1)装置A 适用于过氧化氢与二氧化锰制取氧气,该反应的化学方程式为: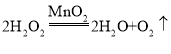 ;
;
(2)实验室常用锌粒与稀硫酸反应制取氢气,该反应属于固液不加热反应,发生装置应选A,氢气难溶于水,密度比空气小,可用排水法或向下排空气法收集,故收集装置应选C或E,故应选择的装置组合是:AC或AE;
(3)其中装置C和装置E不能用来收集二氧化碳,原因是:二氧化碳溶于水,密度比空气大;
(4)饱和碳酸氢钠能与氯化氢气体反应,且不与二氧化碳反应,故如果想除去制取二氧化碳中混有的氯化氢气体,瓶中应盛放饱和碳酸氢钠溶液;洗气应“长进短出”,气体从左通入;
氨气的密度比空气小,如果想用此瓶收集氨气,气体应从右通入;
(二)①由溶解度曲线可知,室温时,碳酸钠的溶解度大于碳酸氢钠,故向等质量的水中加入固体,至固体不能再溶解为止,其中,固体溶解量少的,所对应的物质是NaHCO3,另一种物质是Na2CO3;
②室温时,碳酸钠的溶解度大于碳酸氢钠,故将等质量的碳酸钠和碳酸氢钠配制成饱和溶液,碳酸氢钠所需水的质量大,可设计实验将等质量的碳酸氢钠和碳酸钠配制成室温时的饱和溶液,通过比较所需水的质量多少来区分,实验步骤:取两只试管,分别加入2g碳酸钠和2g碳酸氢钠,分别向两试管中逐步加入蒸馏水,充分振荡、静置、观察现象;现象和结论:至固体完全溶解,其中,消耗蒸馏水多的,所对应的物质是碳酸氢钠,消耗蒸馏水少的,所对应的物质是碳酸钠。