题目内容
【题目】下图中 A﹣L 是初中化学常见的物质。按单质、氧化 物、酸、碱、盐分类,A、B、C、D、E 是五种不同类别的物 质,F 是大理石的主要成分。I 可用于配制农药波尔多液且溶液为 蓝色,K 是红棕色固体。图中“—”表示相连的两种物质之间可 以发生反应,“→”表示物质间存在着相应的转化关系(部分反应 物、生成物及反应条件已略去).
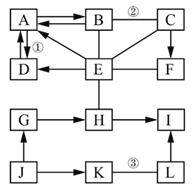
请回答:
(1)写出化学式 F_______ ,G_______ 。
(2)写出反应的化学方程式
②______;③______
(3)反应①的基本反应类型是_______ 。
【答案】 CaCO3 Cu Ca(OH)2+Na2CO3=CaCO3↓+2NaOH Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 分解反应
【解析】F是大理石的主要成分,所以F是碳酸钙;与碳酸钙发生反应的物质是稀盐酸,所以E是稀盐酸;能够生成碳酸钙的反应主要有二氧化碳与氢氧化钙反应、碳酸钠与氢氧化钙反应,所以C是二氧化碳、碳酸钠、氢氧化钙中的一种,由于C与盐酸反应,故C不能是二氧化碳,如果C是氢氧化钙,则B是碳酸钠,A为二氧化碳,D是由盐酸生成的单质为氢气,由于氢气和二氧化碳不能转化,故C不能为氢氧化钙,C为碳酸钠,则D为氢氧化钙;生成氢氧化钙的反应只有氧化钙和水反应,由于A是盐酸生成的,故A是水;D是由盐酸生成的单质为氢气。I 可用于配制农药波尔多液且溶液为蓝色,K 是红棕色固体。故I是硫酸铜,K是氧化铁。H 可以生成硫酸铜,并且 H 可以与酸反应,故H是氧化铜;L 也可以生成CuSO4且能与红棕色固体K反应,则L为H2SO4;J 可以生成 Fe2O3,G 可以生成CuO,且 J 可以反应生成G,得出 J 为 Fe,G 为 Cu。(1)写出化学式 F:CaCO3,G:Cu;(2)反应②是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;反应③是氧化铁与硫酸反应生成硫酸铁和水,反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(3)反应①是水分解生成氢气,该反应的基本反应类型是分解反应。

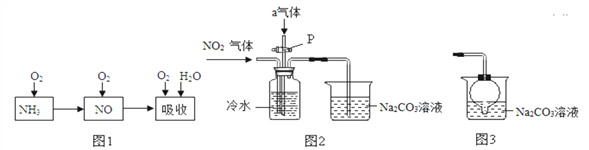
【题目】硼(B)及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和难溶性SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

已知:①Mg2B2O5·H2O+2H2SO4![]() 2MgSO4+2H3BO3②CaSO4微溶于水
2MgSO4+2H3BO3②CaSO4微溶于水
③H2O2溶液可将Fe2+氧化为Fe3+④Fe3+、Fe2+、Al3+以氢氧化物形式开始沉淀和完全沉淀时的pH如下表:
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.14 | 3.0 |
Fe2+ | 5.85 | 8.35 |
Al3+ | 3.0 | 4.7 |
请回答下列问题:
(1)利用______(填物质名称)的磁性,可将该物质直接从“铁硼矿粉”中分离。
(2)酸浸时,矿粉中的金属氧化物会和酸反应,试写出Fe2O3酸浸时的化学反应方程式__________。
(3)为了提高浸出速率(即加快反应速率),除适当增加硫酸浓度外,还可采取的措施有______(写出一条)。
(4)操作a为______,“浸渣”中含有CaSO4和______(填物质化学式)。
(5)“净化除杂”需先加H2O2溶液,然后再调节溶液的pH约为5,目的是_____。
(6)制得的粗硼酸中的主要杂质为________________(填物质化学式)。