题目内容
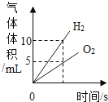
【题目】某同学在进行碳酸钠与酸反应的实验中,发现了一个有趣的现象。当把盐酸溶液逐滴加入到碳酸钠溶液中,开始没有气体产生,一段时间后才有气体产生。查阅资料得知,碳酸钠与盐酸溶液存在两个反应:Na2CO3+HCl═NaHCO3+NaCl;NaHCO3+HCl═NaCl+H2O+CO2↑.他又进行了以下实验:向等体积、含等碳原子数的碳酸氢钠溶液和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,并测得pH与时间的关系,如图甲、乙所示。他们将图甲和图乙的阴影部分进行叠加,发现两者基本重合。
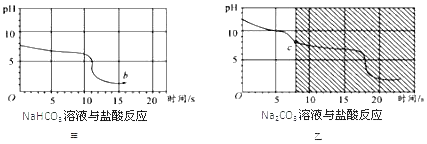
(1)结合图象分析,当把盐酸溶液逐滴加入碳酸钠溶液中,开始没有气体产生的原因是_____。
(2)图甲b点的溶质为_____(写化学式)。
(3)在本实验中加入足量的盐酸产生二氧化碳的量_____。
A 碳酸氢钠多 B 碳酸钠多 C 两者一样多
【答案】碳酸钠与稀盐酸反应生成了碳酸氢钠 HCl、NaCl C
【解析】
(1)分析图像可知,碳酸钠与稀盐酸的反应时,当把盐酸溶液逐滴加入碳酸钠溶液中,开始没有气体产生是因为:碳酸钠与稀盐酸反应先生成了碳酸氢钠。即Na2CO3+HCl═NaHCO3+NaCl。
(2)图甲b点,碳酸氢钠已反应完,由于NaHCO3+HCl═NaCl+H2O+CO2↑,又因为溶液的pH小于7,可见盐酸过量,所以图甲b点的溶质为:HCl、NaCl。
(3)由于向等体积、含等碳原子数的碳酸氢钠溶液和碳酸钠溶液中,加入足量的稀盐酸,由元素守恒可知,在本实验产生二氧化碳的量两者一样多。故选C。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】石灰石是主要矿产品之一,某学校研究性学习小组为了测量当地矿石山石灰石中CaCO3的质量分数,取一些矿石样品,并取稀盐酸200g,平均分成4份,分4次进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
问:(1)哪几次实验中矿石有剩余?_____。
(2)表中m的数值是_____。
(3)试计算这种石灰石中CaCO3的质量分数_____。
(4)试计算这种稀盐酸溶质的质量分数_____。