题目内容
3月22日是 “世界水日”。关于水的知识,请回答下列问题:
(1)下列净水方法中,生产自来水使用的方法有(填字母序号)
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
(2)实验室常用过滤的方法对液体进行提纯,在此操作中需要用到的玻璃仪器有:玻璃棒、烧杯、__________(填仪器名称);生活中常用 的方法将硬水软化。
(3)有关水的组成和结构的叙述中,正确的是(填字母序号)
A.水是由水分子构成的
B.水分子的相对分子质量是18g
C.水中氢、氧元素的质量比为2:1
D.水分子是由氢原子和氧原子构成的
(4)下列示意图①~③中,“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子。
”表示氧原子。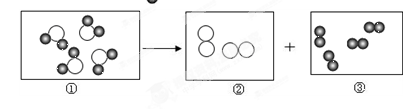
表示化合物的是(填序号) ,③所代表的物质是图中 试管(填字母)中产生的气体,图中A是电源的 极(填“正”或“负”) 极。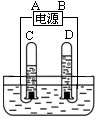
(5)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,写出该反应的化学方程式 。
(1)ABE;(2)漏斗;煮沸;(3)AD;(4)①;C;负极;(5)2H2O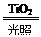 2H2↑+O2↑.
2H2↑+O2↑.
解析试题分析:(1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附、消毒杀菌;
(2)过滤需要的玻璃仪器有:烧杯、漏斗、玻璃棒;生活中常用煮沸的方法将硬水中的钙、镁离子沉淀下来,达到软化水的目的;
(3)A.水是由水分子构成的,正确;
B.水分子的相对分子质量是:2+16=18,单位是1,省略不写,故错误;
C.水中氢、氧元素的质量比为1×2:16=1:8,而不是2:1,故错误;
D.水分子是由氢原子和氧原子构成,正确;
(4)化合物是纯净物,所以化合物中只有一种分子,且分子中含有多种原子,分析图示中分子的情况可知构成化合物分子的是图①;③所代表的物质是由分子构成,是每个分子由两个氢原子构成的氢分子,氢分子构成氢气,氢气多,大约是氧气体积的2倍,是在负极得到的;
(5)在TiO2作催化剂和光照条件下,水分解成氢气和氧气,反应的化学方程式是:2H2O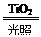 2H2↑+O2↑
2H2↑+O2↑
考点:自来水的生产过程与净化方法;过滤的原理、方法及其应用;电解水实验;水的组成;硬水与软水;微粒观点及模型图的应用

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案(6分)现有六种物质,选择相应物质的字母填空
| A.活性炭 | B.高锰酸钾 | C.石油 | D.聚乙烯塑料 E.干冰 F.酒精 |
(3) 被誉为“工业的血液” (4) 可用于吸附冰箱内的异味
(5) 可用于实验室制取氧气 (6) 可用作食品包装袋