题目内容
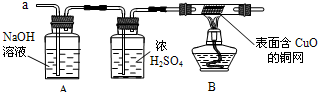
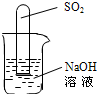
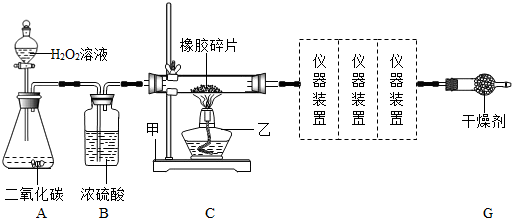
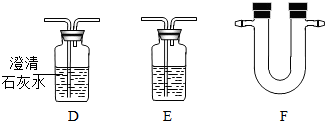
某固体可能含有C、Fe2O3、CuO、CaCO3中的一种或几种.取该固体物质在隔绝空气的条件下加强热,产生的气体能使澄清的石灰水变浑浊.再把强热后的固体残渣冷却后投入足量的稀盐酸中,残渣全部溶解,并产生一种可燃性气体.由此推断该固体物质中一定含有 ,一定不含有 ,可能含有 .
【答案】分析:能够使澄清石灰水变浑浊的气体是二氧化碳,在高温的条件下加热固体混合物能够产生二氧化碳的组合可能是:①碳酸钙②碳和氧化铜③碳和氧化铁等,根据第二步向残渣中加入稀盐酸后产生了一种具有可燃性的气体,根据题给的物质可以判断在残渣中含有铁单质,所以在混合物中就有氧化铁.
解答:解:由实验步骤(1)的现象说明:样品在高温条件下产生了二氧化碳.
该二氧化碳可能是由碳酸钙分解产生,也可能是碳与氧化铜或氧化铁反应产生,或与两者都反应产生,若是有后者发生,则同时会生成铜或铁,或两者都有生成.
由实验步骤(2)的现象说明:由残渣全部溶解说明生成物中一定没有铜,说明固体混合物中一定没有氧化铜;产生的可燃性气体是氢气,由氢气的产生说明生成物中一定含有铁,说明固体混合物中一定含有炭粉和氧化铁.但有没有碳酸钙,由于没有相关现象说明,因此断定固体混合物中可能含有碳酸钙.
故答案为:C、Fe2O3;CuO;CaCO3
点评:本题是推断题,解答该类题目的关键是找准突破口,然后根据具体的实验来做出推断和猜测,只要我们的猜测能够自圆其说,经得起挑剔,那么我们的解答就是正确的.
解答:解:由实验步骤(1)的现象说明:样品在高温条件下产生了二氧化碳.
该二氧化碳可能是由碳酸钙分解产生,也可能是碳与氧化铜或氧化铁反应产生,或与两者都反应产生,若是有后者发生,则同时会生成铜或铁,或两者都有生成.
由实验步骤(2)的现象说明:由残渣全部溶解说明生成物中一定没有铜,说明固体混合物中一定没有氧化铜;产生的可燃性气体是氢气,由氢气的产生说明生成物中一定含有铁,说明固体混合物中一定含有炭粉和氧化铁.但有没有碳酸钙,由于没有相关现象说明,因此断定固体混合物中可能含有碳酸钙.
故答案为:C、Fe2O3;CuO;CaCO3
点评:本题是推断题,解答该类题目的关键是找准突破口,然后根据具体的实验来做出推断和猜测,只要我们的猜测能够自圆其说,经得起挑剔,那么我们的解答就是正确的.

练习册系列答案
相关题目