题目内容
我区石灰石资源丰富,某县为开发本地石灰石资源,招商广告称“本县石灰石资源丰富,品质优良,碳酸钙含量不低于85%”.一投资商派技术员到该地取回样品,从中称取12.5g与稀盐酸完全反应(杂质不参加反应),测得生成二氧化碳的质量为4.4g.根据检测获得的数据计算并判断样品中碳酸钙的质量分数与实际是否相符.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式,利用反应产生的二氧化碳气体的质量可计算参加反应的盐酸的质量及碳酸钙的质量;
利用样品中碳酸钙的质量分数=
×100%,可求得样品中碳酸钙的质量分数,并与广告中碳酸钙含量进行比较,以判断广告的真实性.
利用样品中碳酸钙的质量分数=
| 碳酸钙的质量 |
| 样品的质量12.5g |
解答:解:设参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 4.4g
=
x=10g
样品中碳酸钙的质量分数=
×100%=80%
广告中“碳酸钙含量不低于85%”的宣传不真实
答:该广告不是真实的.
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g
样品中碳酸钙的质量分数=
| 10g |
| 12.5g |
广告中“碳酸钙含量不低于85%”的宣传不真实
答:该广告不是真实的.
点评:利用反应的化学方程式表示物质的质量关系,根据反应中某一物质的质量可计算反应中其它任何物质的质量.

练习册系列答案
相关题目

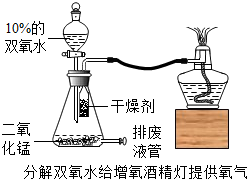 徐州市化学教师李老师发明了如下图所示的增氧酒精灯,使用时将二氧化锰催化双氧水产生的氧气通入灯芯座的增氧孔,这时能观察到焰心的酒精剧烈燃烧,火焰发白.
徐州市化学教师李老师发明了如下图所示的增氧酒精灯,使用时将二氧化锰催化双氧水产生的氧气通入灯芯座的增氧孔,这时能观察到焰心的酒精剧烈燃烧,火焰发白.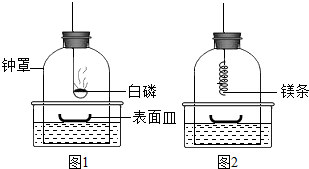 实验课上,为检验镁条能否在N2中燃烧,兴趣小组的同学展开如下探究:
实验课上,为检验镁条能否在N2中燃烧,兴趣小组的同学展开如下探究: