题目内容
【题目】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开始实验探究。
【猜想假设】
猜想(1):该溶液没有变质,该溶液的溶质为_____________。
猜想(2):该溶液全部变质,该溶液的溶质为_____________。
猜想(3):该溶液部分变质,该溶液的溶质为NaOH和Na2CO3的混合溶液。
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
实验操作 | 可能出现的现象与结论 | 同学评价 | |
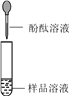
第1组 |
| 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:__________。 |
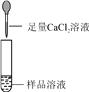
第2组 |
| 若产生白色沉淀,反应方程式是:________ ,则猜想_______不成立。 | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立。 |
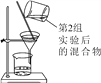
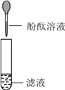
第3组 | 第一步 第二步
| 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立。 | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:_____________ |
【探究实验】综合各小组的方案后,动手实验。
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要______________保存。
【答案】 NaOH Na2CO3 Na2CO3溶液呈碱性 CaCl2+ Na2CO3=CaCO3↓+2 NaCl 则猜想(1)不成立 直接向变浑浊的溶液中直接滴加酚酞溶液 密封保存
【解析】【猜想假设】
猜想(1):NaOH溶液没有变质,该溶液的溶质为NaOH;
猜想(2):NaOH溶液全部变质,说明和空气中的CO2反应全部生成了碳酸钠,则溶液的溶质为Na2CO3 ;
【设计方案】
第1组:碳酸钠溶液呈碱性,也能使酚酞试液变红,故填:碳酸钠溶液呈碱性;
第2组:碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,反应方程式为CaCl2+ Na2CO3=CaCO3↓+2 NaCl ,加入氯化钙溶液产生沉淀,说明含有碳酸钠,猜想(1)不成立;
第3组:第2组实验结束后,让试管静置一段时间,取上层清液滴加酚酞溶液即可,故填:直接向变浑浊的溶液中直接滴加酚酞溶液即可;
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存,防止变质。

 期末集结号系列答案
期末集结号系列答案【题目】下列事实的解释合理的是
事 实 | 解 释 | |
A | 淀粉没有甜味 | 淀粉不属于糖类 |
B | 打开汽水瓶盖时,汽水会自动喷出来 | 压强减小,气体在水中的溶解度变小 |
C | 洗洁精可以去除油污 | 洗洁精溶解了油污 |
D | 过滤时使用玻璃棒 | 玻璃棒起搅拌作用 |
A. A B. B C. C D. D