题目内容
【题目】一定条件下,同一化学反应进行的快慢与反应物的质量分数成正比。现用100g溶质质量分数为30%的盐酸溶液与过量的锌粉反应,为了使反应慢点儿进行,而又不影响生成氢气的总量,可向所用的盐酸中加入适量的
A. 氢氧化钠 B. 水 C. 氧化镁 D. 碳酸钠溶液
【答案】B
【解析】金属与酸反应,生成氢气的质量等于酸中氢元素的质量。使反应慢点儿进行,而又不影响生成氢气的总量,所以加入的物质只能降低酸的浓度,不能消耗酸中的氢离子。加入氢氧化钠反应实质是氢离子和氢氧根离子结合生成水分子,不符合要求;加水时,只能降低酸的浓度,不能消耗酸中的氢离子,符合要求;氧化镁和酸反应生成盐和水;碳酸钠和酸反应生成盐、二氧化碳、水。选B

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开始实验探究。
【猜想假设】
猜想(1):该溶液没有变质,该溶液的溶质为_____________。
猜想(2):该溶液全部变质,该溶液的溶质为_____________。
猜想(3):该溶液部分变质,该溶液的溶质为NaOH和Na2CO3的混合溶液。
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
实验操作 | 可能出现的现象与结论 | 同学评价 | |
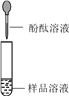
第1组 |
| 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:__________。 |
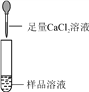
第2组 |
| 若产生白色沉淀,反应方程式是:________ ,则猜想_______不成立。 | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立。 |
第3组 | 第一步 第二步
| 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立。 | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:_____________ |
【探究实验】综合各小组的方案后,动手实验。
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要______________保存。