题目内容
(2007?宿迁)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.(1)现选择合适的装置来制取并收集NH3,应该选择的发生装置是,收集装置是.
(2)若用湿润的红色石蕊试纸来检验NH3,产生的现象是.
(3)工业上采用氨氧化法制硝酸,该工业生产的第一步反应为4NH3+5O2
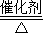 4X+6H2O,则X的化学式为.
4X+6H2O,则X的化学式为.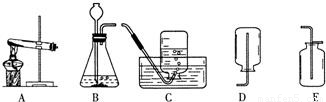
【答案】分析:(1)根据反应物的状态和反应条件确定发生装置,根据气体的密度和溶水性确定收集装置.
(2)根据酸碱指示剂遇酸碱溶液的变色情况进行分析.
(3)根据质量守恒定律,化学反应前后原子的种类和数目都不变.
解答:解:(1)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;氨气极易溶于水,密度比空气小,应用向下排空气法收集.故答案为:A; D
(2)氨气的水溶液显碱性,碱溶液能使石蕊试纸变蓝.故答案为:湿润的红色石蕊试纸变蓝
(3)反应物中的原子的种类和个数为:4N,12H,10O,根据质量守恒定律,生成物中也应有同样的原子,生成物中已知的原子种类和个数为12H,6O,剩余的4N和4O构成了4X,则一个X分子由一个氮原子和一个氧原子构成,X的化学式为:NO
点评:气体的收集方法主要由气体的密度和溶水性决定,另外还要考虑气体是否有毒、是否与空气中的物质反应等.氨气有刺激性气味,会污染空气,所以用向下排空气法收集氨气时最好再加一个尾气处理装置.
(2)根据酸碱指示剂遇酸碱溶液的变色情况进行分析.
(3)根据质量守恒定律,化学反应前后原子的种类和数目都不变.
解答:解:(1)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;氨气极易溶于水,密度比空气小,应用向下排空气法收集.故答案为:A; D
(2)氨气的水溶液显碱性,碱溶液能使石蕊试纸变蓝.故答案为:湿润的红色石蕊试纸变蓝
(3)反应物中的原子的种类和个数为:4N,12H,10O,根据质量守恒定律,生成物中也应有同样的原子,生成物中已知的原子种类和个数为12H,6O,剩余的4N和4O构成了4X,则一个X分子由一个氮原子和一个氧原子构成,X的化学式为:NO
点评:气体的收集方法主要由气体的密度和溶水性决定,另外还要考虑气体是否有毒、是否与空气中的物质反应等.氨气有刺激性气味,会污染空气,所以用向下排空气法收集氨气时最好再加一个尾气处理装置.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

