题目内容
【题目】可溶性酸、碱、盐在水中可解离出阴阳离子,我们现阶段所学的复分解反应的实质就是酸、碱、盐解离出的一些阴、阳离子相互结合生成难解离的水、气体或沉淀,根据如下所列溶解性表及氢氧化钠溶液和盐酸反应的微观示意图回答问题。
部分碱和盐的溶解性表(20℃)
阴离子 | 阳离子 | ||
Na+ | K+ | Ba2+ | |
OH- | 溶 | 溶 | 溶 |
SO42- | 溶 | 溶 | 不溶 |
CO32- | 溶 | 溶 | 不溶 |
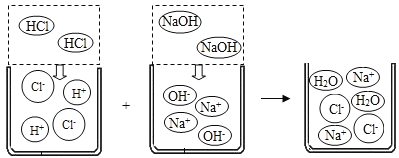
(1)如上图所示,HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推H2SO4在水中会解离出的离子是____________(填离子符号)。
(2)根据上述微观示意图写出化学反应方程式____________,判断反应前后溶液中数目发生变化的离子是____________(填离子符号)。
(3)根据溶解性表及复分解反应的实质判断,将“H2SO4、BaCl2、NaOH、K2CO3”四种物质的溶液两两混合,能发生的反应有________________________个。
【答案】H+、SO42- HCl+NaOH═NaCl+H2O H+、OH- 4
【解析】
(1)根据HCl、NaOH解离,发现物质解离规律,判断H2SO4在水中会解离出的离子.
(2)观察微观示意图,判断所发生的反应,写出反应的化学方程式,并对比反应前后的图示,找出反应前后溶液中数目发生变化的粒子。
(3)利用复分解反应发生的条件,判断“硫酸、氯化钡、氢氧化钠、碳酸钾”四种物质的溶液两两混合,所能发生的反应.
(1)由HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,可得知解离时原子团并不分开,因此H2SO4在水中会解离出氢离子和硫酸根离子,两种离子的符号分别为H+、SO42-;故填:H+、SO42-。
(2)图示反应前后的反应物为HCl和NaOH,反应后为H2O和NaCl在水中解离出的Na+和Cl-,所以反应的化学方程式为HCl+NaOH═NaCl+H2O;反应前H+、OH-在反应后不存在,而反应后出现了H2O,反应前后Na+和Cl-不变,所以反应前后溶液中数目发生变化的离子是H+、OH-;故填:HCl+NaOH═NaCl+H2O;H+、OH-。
(3)硫酸与氯化钡可产生硫酸钡沉淀、与氢氧化钠可形成水、与碳酸钾可生成水与二氧化碳,氯化钡与碳酸钠可形成碳酸钡沉淀,符合复分解反应产生水或气体或沉淀的发生条件,而氯化钡与氢氧化钠、氢氧化钠与碳酸钠因不能形成气体、水或沉淀而不能发生复分解反应,因此“硫酸、氯化钡、氢氧化钠、碳酸钾”四种物质的溶液两两混合,共能发生4个反应;故填:4。

 阅读快车系列答案
阅读快车系列答案