题目内容
【题目】现有一根质量为33.6g表面被氧化的的铜丝,完全浸没在烧杯中的l00g稀硫酸里,恰好完全反应后将铜丝取出(不考虑实验中的损失),称量,烧杯中物质的质量为108g,则原铜丝中未被氧化的铜占原铜丝质量的( )
A. 20% B. 50% C. 80% D. 90%
【答案】C
【解析】
现有一根质量为33.6g的表面被氧化的铜丝,其组成为Cu和CuO,CuO和硫酸反应会生成硫酸铜和水,而Cu不会与硫酸反应,所以恰好完全反应后增加的质量就是氧化铜的质量,则氧化铜的质量为:108g-100g=8g,CuO中铜的质量为:8g×![]() =6.4g,原铜丝的质量为:33.6g-(8g-6.4g)=32g,所以原铜丝中未被氧化的铜占原铜丝的质量分数为:
=6.4g,原铜丝的质量为:33.6g-(8g-6.4g)=32g,所以原铜丝中未被氧化的铜占原铜丝的质量分数为:![]() ×100%=80%。故选C。
×100%=80%。故选C。

【题目】(1)分类是学习化学常用的方法。
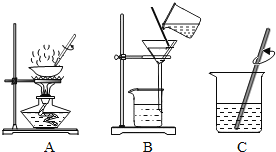
初中化学有许多实验,有的实验侧重于观察和描述,属于观察和描述型实验;有的实验侧重于对一个问题采用控制变量的方法系统探究,属于问题探究型实验。据此可将实验B与实验①_____归为一类。分类的依据是:②___________________________。
蜡烛及其燃烧的探究 |
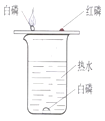
探究可燃物燃烧的条件 |
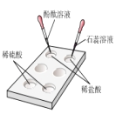
酸、碱与指示剂作用 |
铁制品锈蚀的条件 |
A | B | C | D |
(2)在九年化学书附录I部分,酸、碱、盐的溶解性表中,有些物质溶解性用“—”表示,说明该物质不存在或遇到水就会发生“水解”反应。
例如碳酸铝遇水就会发生“水解”反应:Al 2(CO3)3+ 3H2O==2Al(OH)3↓ + 3CO2↑,据此信息请同学们写出碳酸铁(其中铁元素的化合价与碳酸铝中铝元素的化合价相同)“水解”反应的化学方程式①____________________________,反应过程中观察到的实验现象有②__________________________(答两点)。