题目内容
【题目】化学能帮助我们更好地认识生活、改善生活.

(1)现有六种物质:A硝酸钾 B小苏打 C熟石灰 D甲烷 E生石灰 F碳酸钙.试按下列要求用序号填空:
①常用作干燥剂的是________;
②常用作发酵粉主要成分的是________;
③天然气的主要成分是________;
④常用作改良酸性土壤的碱是________.
(2)乘车禁止携带物品的部分标识如图所示.在浓硫酸、食盐、汽油、纯碱四种物品中,不宜携带上车的是________、________.
(3)某胃药的主要成分是Al(OH)3, 常用于治疗胃酸过多,写出其与胃酸反应的化学方程式是________.
(4)秋葵是一种大众喜爱的食材,含有蛋白质、维生素、果糖和丰富的铁、锌、钙等元素,其中属于人体所需常量元素的是________.
【答案】EBDC浓硫酸汽油3HCl+Al(OH)3=AlCl3+3H2O钙
【解析】
(1)
①生石灰能和水反应生成氢氧化钙,故常用作干燥剂,故选E;
②小苏打学名碳酸氢钠,受热分解出二氧化碳,故常用作发酵粉主要成分,故选B;
③天然气的主要成分是甲烷,故选D;
④常用作改良酸性土壤的碱是熟石灰,是一种碱,能中和土壤中的酸性物质,故选C;
(2)浓硫酸具有腐蚀性,汽油属于易燃物质,故浓硫酸、汽油不能不以携带上车;
(3)胃酸主要成分是盐酸,故会发生酸碱中和,化学方程式为3HCl+Al(OH)3=AlCl3+3H2O;
(4)人体的牙齿、骨骼中含有大量的钙元素,故钙元素属于人体所需常量元素。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】下图为某钙片标签上的部分文字,请仔细阅读后回答下列问题。
(1)维生素D种类较多,其中维生素D2的化学式为C28H44O,试计算:
①维生素D2的相对分子质量________________;
②维生素D2中碳、氢、氧三种元素的质量比________________;
(2)计算每片钙片中含碳酸钙(CaCO3)的质量。_____________
(主要原料)碳酸钙、维生素D (功效成分)补钙 |
每片含钙(以Ca计)500 mg、维生素D100ug (食用方法)每日一次,每次一片 (规 格)2.5g/片 |
【题目】碳酸钠广泛用于造纸、纺织、玻璃、洗涤剂、肥皂、制革等工业,是一种重要的化工原料。吕布兰、索尔维和侯德榜为碳酸钠的工业化生产作出了巨大贡献。
Ⅰ、吕布兰法
1789年,法国医生吕布兰(N.Leblanc,1742—1806)以食盐、浓硫酸,木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如下:

(1)碳酸钠俗称______。
(2)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为______。
(3)③中“水浸”时通常需要搅拌,其目的是______。
(4)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处______。
Ⅱ、索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,2NaHCO3![]() Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
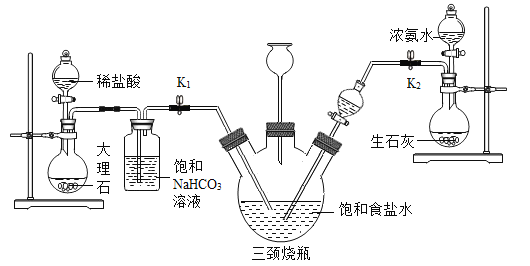
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
请回答下列问题:
(5)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为______。
(6)三颈烧瓶上连接的长颈漏斗的主要作用是______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通一段时间
CO2,其目的是______。
(7)根据实验记录,计算t2时NaHCO3固体的分解率______(已分解的NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程。若加热前NaHCO3固体中还存在少量NaCl,上述计算结果将_____(填“偏大”、“偏小”或“无影响”)。
(8)制碱技术在很长一段时间内把持在英、法等西方国家手中,我国化学工程专家侯德榜先生独立摸索出索尔维法并公布于众,又于1943年创造性地将制碱与制氨两种工艺联合起来,基本消除废弃物的排放,同时生产出碳酸钠和氯化铵两种产品,这就是著名的候氏制碱法。下列认识或理解正确的是______。
①科学认识是在曲折的、艰辛的积累过程中不断进步的;
②“科技兴邦、实业救国”是侯德榜先生回国研究的巨大动力;
③侯氏制碱法大大提高了原料的作用率,它符合当今“绿色化学”的理念。
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成,同学们查阅资料得知NaCl、CaCl2、BaCl2等溶液呈中性,经过思考,设计并进行了以下实验:
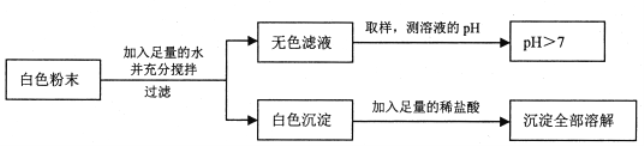
(1)白色粉末一定不含_____________,可能含有______________。
(2)为了确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(猜想假设)猜想一:NaOH
猜想二:______________
猜想三:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 结论 |
1.取少量该溶液于试管中 滴入_________溶液。 | _____________ | 猜想三正确 |
2.静置上述溶液,取少量上层清液于另一试管中,滴入几滴___________溶液。 | _______________ |
步骤1中发生反应的化学方程式为_______________。
(得出结论)白色粉末的成分是_________________。