题目内容
【题目】写出下列反应的化学方程式.
(1)锌和稀硫酸反应__________________________________。
(2)含氢氧化铝的药物治疗胃酸过多症_____________________。
(3)生锈的铁器用稀盐酸“酸洗”______________________。
(4)工业上通过电解饱和食盐水得到氢氧化钠、氯气和氢气________________。
(5)放置在空气中的装有澄清石灰水试剂瓶口白色固体的形成_____________。
【答案】 (1)Zn+H2SO4=ZnSO4+H2↑ (2)Al(OH)3+3HCl=AlCl3+3H2O (3)Fe2O3+6HCl=2FeCl3+3H2O (4)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ (5)CO2+Ca(OH)2=CaCO3↓+H2O
2NaOH+H2↑+Cl2↑ (5)CO2+Ca(OH)2=CaCO3↓+H2O
【解析】(1)锌和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式:Zn+H2SO4=ZnSO4+H2↑;(2)氢氧化铝与胃酸中的盐酸生成氯化铝和水,反应的化学方程式:Al(OH)3+3HCl=AlCl3+3H2O;(3)铁锈中的氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式:Fe2O3+6HCl=2FeCl3+3H2O;(4)电解饱和食盐水生成氢氧化钠、氯气和氢气,反应的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(5)澄清石灰水与空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O。
2NaOH+H2↑+Cl2↑;(5)澄清石灰水与空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O。

【题目】某实验小组取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,于是小组中的几位同学对其中的成分进行了探究。

(提出猜想)小丹认为含有:CaO、Ca(OH)2;
小凯认为含有:CaO、Ca(OH)2、CaCO3;
小欣认为含有:Ca(OH)2、CaCO3。
(设计实验)
实验操作 | 实验现象 | 结论 | |
步骤一 | 取试样于试管中加水振荡 | 液体浑浊,用手摸试管外壁,感觉不发热 | ______________________ |
步骤二 | 向步骤一的试管中滴加无色酚酞溶液 | 溶液变红色 | ______________________ |
步骤三 | _______________________ | 试管内有气泡生成 | 一定含有CaCO3 |
(得出结论)通过以上探究可知_________同学的猜想正确,请写出使CaO变质的化学方程式:______。
(拓展)如果生石灰已全部变质为碳酸钙,请你设计实验加以证明(写出必要的步骤、现象和结论)___。
【题目】实验室需配置一定浓度的硝酸钾溶液。
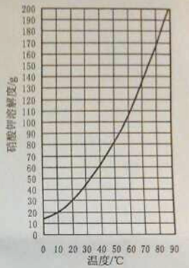
(1) 查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配置40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
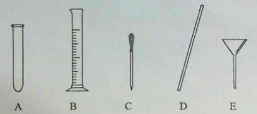
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位1g/mL)
质量分数/% | 20 | 40 | 60 |
4 | 1.023 | 1.016 | 1.007 |
10 | 1.063 | 1.054 | 1.044 |