题目内容
【题目】根据如图所示的实验回答问题。
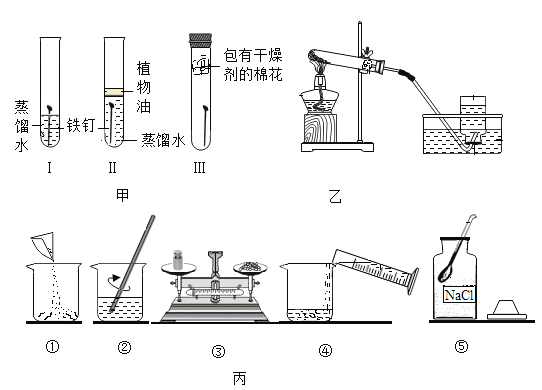
(1)甲实验中I和II对比,可以得出铁生锈的条件是_______________,II中蒸馏水需要煮沸并覆盖一层植物油的目的是_________________。
(2)乙实验是高锰酸钾制取氧气的装置图,此实验中试管口处棉花的作用______________。
(3)丙实验是配制一定溶质质量分数的氯化钠溶液,请指出图中的一处错误:_____________,改正错误后,实验步骤为______________。
【答案】需要与氧气接触 除去水中溶解的氧气,防止铁钉与氧气接触 防止高锰酸钾粉末进入导管,造成导管堵塞 使用托盘天平称量时未遵循“左物右码”的原则(或使用托盘天平时药品和砝码放反了) ⑤③①④②
【解析】
(1)甲实验中: I试管内铁钉与水和氧气同时接触而生锈; II试管中铁钉只与水接触不生锈,所以两者对比说明铁钉生锈需要与氧气接触。蒸馏水煮沸过程中,氧气从水中逸出,植物油覆盖在水面防止空气中的氧气溶于水,使Ⅱ中的铁钉只与水接触。
(2)用高锰酸钾制取氧气时,在试管口加一团棉花的作用是防止高锰酸钾粉末进入导管,造成导管堵塞。
(3)使用托盘天平称量时应遵循“左物右码”的原则,配制一定溶质质量分数溶液的步骤是:计算、称量、量取、溶解,故填⑤③①④②。

 名校课堂系列答案
名校课堂系列答案【题目】碳酸氢铵是一种常用的化肥,小组同学对碳酸氢铵进行相关的探究:
[查阅资料](1)碳酸氢铵是一种白 色粒状晶体,有氨臭,易溶于水。
(2)氨气具有刺激性气味,极易溶于水。
[提出问题]碳酸氢铵有哪些化学性质?
[作出猜想]猜想一:碳酸氢铵能与酸反应;
猜想二:碳酸氢铵能与碱反应;
猜想三:碳酸氢铵易分解。
[设计与实验]
实验操作 | 实验现象 | 实验结论 | |
1 | _____ | 有气泡产生 | 猜想一正确 |
2 | 取少量碳酸氢铵样品与熟石灰混合研磨 | _____。 | 猜想二正确 |
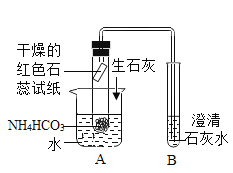
3 |
| 红色石蕊试纸变蓝,澄清石灰水变浑浊 | 猜想三正确, B中发生反应的化学方程式为_____。 |
[反思](1)实验3中向水中加入氧化钙的目的是_____。
(2)有同学对实验2的结论提出质疑:碳酸氢铵易分解产生有刺激性气味的气体,研磨会使温度升高,能加快碳酸氢铵分解,所以实验2的结论不严谨。
[补充探究]有同学为了进一步验证猜想二,进行如下实验:
实验操作 | 实验现象 |
①将碳酸氢铵溶液加入到氢氧化钙溶液中 | 有白 色沉淀生成,但没有气体逸出 |
②将碳酸氢铵溶液加入到氢氧化钠溶液中 | 有刺激性气味的气体生成 |
[分析]根据常见酸、碱、盐的溶解性分析,①实验中生成的白色沉淀是_____,实验中没有气体逸出可能的原因是_____。
[实验结论]三个猜想均正确。
[拓展应用]保存或使用碳酸氢铵时,需注意_____(写出一点)。
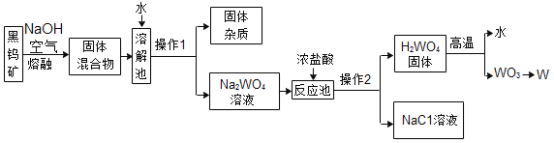
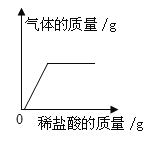
【题目】石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应)。课外小组同学将50g盐酸均分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
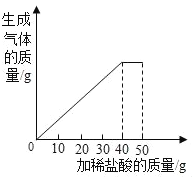
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 16 | 12 | 8 |
请计算:
(1)石灰石样品中杂质的质量为_____g。
(2)所加盐酸的溶质质量分数_____。
(3)实验室只提供溶质质量分数为36.5%的盐酸,欲配制该实验所用的50克盐酸,需要36.5%的盐酸和水各多少克?_____
【题目】实验课上,李杰拿出一片黄色的金属向同学炫耀说他捡到了黄金,张峰说他曾在网上看到过,有一种铜锌合金外观和黄金相似,常被误认为是黄金。于是他与李杰开始探究。
(提出问题)这块黄色金属是黄金?还是铜锌合金?
(猜 想)①李杰认为是黄金 ②张峰认为是铜锌合金
(查阅资料)合金中的金属保持各自的化学性质,金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
(设计实验)李杰设计的实验是:截取一小片黄色的金属放在石棉网上用酒精灯加热;张峰设计的实验是:截取一小片黄色的金属放入硝酸银溶液中。
(现象与结论)李杰在实验中观察到黄色的金属变黑,则他的猜想_____(填“正确”或“错误”),黑色物质是_____。张峰在实验中观察到的现象是_____,反应的化学方程式为_____(只写一个)。
(反思与应用)假如你与张峰的观点相同,请你设计另一实验方案并完成下列实验报告。
实验操作 | 实验现象 | 化学方程式 |
截取一小片黄色金属放入_____溶液中. | _____ | _____ |