题目内容
【题目】某化学研究小组的同学欲对某种塑料袋的组成进行分析研究,并测算元素的质量分数,设计了如图所示的实验装置.
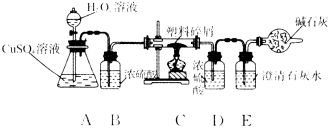
(提示:资料显示该种塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水.图中碱石灰可以吸收空气中的二氧化碳与水蒸气)
(1)实验时,打开分液漏斗的活塞,将H2O2:溶液滴入到A装置的________(填仪器名称)中,再点燃C处的酒精灯,使反应进行.
(2)A装置中CuSO4溶液的作用是________.
(3)通过观察到________________的现象,可以判断塑料袋试样中含有碳元素.
(4)根据实验前后D装置的质量变化测算出该塑料袋试样中氢元素的质量分数为14.3%.若装置中没有连接仪器B,则测算出来的氢元素的质量分数会________________(填“偏大”“偏小”或“不变”).
【答案】(1)锥形瓶
(2)催化作用
(3)E装置中澄清石灰水变浑浊
(4)偏大
【解析】本题关键是明确实验的原理和每个装置的作用.塑料燃烧产生二氧化碳和水,浓硫酸吸收水,澄清的石灰水检验二氧化碳.D中浓硫酸增加的质量为生成水的质量,由水的质量可求出氢元素质量.装置A是氧气发生装置,硫酸铜溶液是催化剂;B是干燥装置.若无B装置,则氧气中含的水蒸气也被D吸收,则求出的氢元素的质量分数将偏大.

练习册系列答案
相关题目

