��Ŀ����
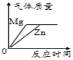
����Ŀ��ij��ѧ��ȤС��Ϊ�˲ⶨһ��ʯ��ʯ��Ʒ��̼��Ƶ�����������ȡ��2gʯ��ʯ��Ʒ����20gϡ�����4�μ�����Ʒ�У���Ʒ�г�̼����⣬����ijɷּȲ������ᷴӦ��Ҳ������ˮ����ÿ�γ�ַ�Ӧ�����ˡ������������ʵ���������£�
ʵ����� | 1 | 2 | 3 | 4 |
ϡ��������� | 5g | 5g | 5g| | 5g |
ʣ���������� | 1.5g | 1.0g | 0.5g | 0.3g |
��1�����������ݿ�֪�����Ĵ�ʵ���У���______��ʯ��ʯ��Ʒ�е�̼�������ȫ��Ӧ��
��2��ʯ��ʯ��Ʒ��̼��Ƶ�����������_______��
��3�����һ��ʵ�������CO2��������______��Ҫ��д��������̣�
���𰸡�4 85% 0.22g
��������
����ͼ��ǰ����ÿ�ι������0.5g�������Ĵ�ֻ������0.2g��˵�����Ĵ�̼����Ѿ���ȫ��Ӧ��ʣ���Ϊ���ʣ�̼��Ƶ�����Ϊ2g-0.3g=1.7g���ݴ˼��㡣
(1)��1��2��3��ʵ���֪��ÿ�η�Ӧ��̼���������0.5g������4�η�Ӧ��̼���������0.2g��˵����4����̼����Ѿ���ȫ��Ӧ��
(2)ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ��![]() ��
��
(3)���һ�β���������̼����Ϊx��
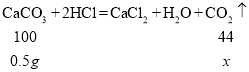
![]()
x=0.22g
�����һ��ʵ�������CO2������Ϊ0.22g��

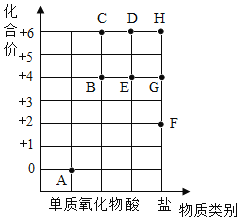
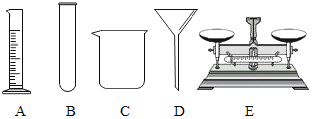
 �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д� ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д�����Ŀ��ˮ������֮Դ������Ӧ���˽�ˮ����Һ�����֪ʶ��
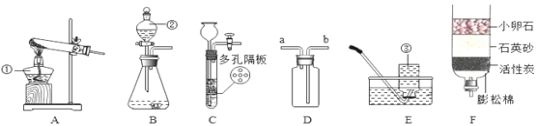
��1�������п���_____����Ӳˮ����ˮ��
��2����ˮʱ�����û���̿��_____�Գ�ȥˮ�е�ɫ�غ���ζ��
��3���»����Ȼ��ƺ�������ڲ�ͬ�¶ȵ��ܽ����ش�
�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
�ٸ����ϱ����ݷ���NaCl��KNO3���ܽ����ȵ��¶���_____������ĸ ��֮�䡣
A 10�橁20�� B 20�橁30�� C 30�橁40��
����NaCl�л���������KNO3���ᴿNaCl�ķ�����_____��
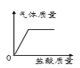
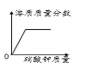
��ijͬѧȡNaCl��KNO3�е�һ�����ʣ�����ͼ��ʾ����ʵ�顣
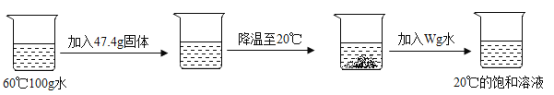
��ͬѧ��ȡ�Ĺ�������Ϊ_____��W��ֵΪ_____g��