题目内容
【题目】下列实验现象描述正确的是
A. 打开盛有浓盐酸的瓶盖,瓶口出现白烟
B. 铜丝浸入硝酸银溶液中,溶液由蓝色变无色
C. 二氧化碳通入石蕊溶液中,溶液由红色变紫色
D. 氯化铵和熟石灰混合研磨,闻到刺激性气味
【答案】D
【解析】
试题分析:A. 打开盛有浓盐酸的瓶盖,瓶口出现白雾[。此项错误。
B. 铜丝浸入硝酸银溶液中,溶液由无色(硝酸银溶液)变蓝色(硝酸铜溶液)。此项错误。
C. 二氧化碳通入石蕊溶液中,二氧化碳与水反应碳酸(溶液呈酸性)可使紫色的石蕊试液变红。此项错误。
D. 氯化铵和熟石灰混合研磨,可生成有刺激性气味的氨气。此项正确。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
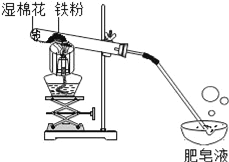
(1)试管尾部放一团湿棉花的目的是____________.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是____________.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是__.
【实验探究】
实验操作 | 实验现象及结论 |
______________ | ________________ |
【实验结论】铁和水蒸气反应的化学方程式为__.
【反思与交流】该黑色固体不可能是Fe2O3,理由是__.