题目内容
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答: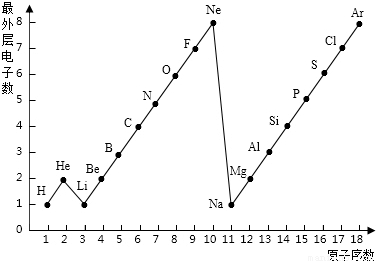
(1)第三周期11一18号元素原子最外层电子数变化的趋势是______.
(2)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系.在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钾元素(原子序数为19)单质与水反应的生成物.甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为______同学的猜想不合理,请从化合价的角度解释原因
______.
【答案】分析:(1)直接根据图示可知道其变化趋势;
(2)根据题意可知“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”,结合这句话从化合价的升高和降低来分析即可.
解答:解:(1)从图示可看出11--18号元素原子最外层电子数变化的趋势是:逐渐递增(或从1到8逐渐递增).
(2)乙同学的猜想不合理.
原因:若生成KOH和O2,则该反应中钾元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低.
故答案为:
(1)逐渐递增(或从1到8逐渐递增).
(2)乙;若生成KOH和O2,该反应中钾元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低.
点评:主要考查了化合价规律和原则,粒子结构示意图.要能准确的读图,认真阅读并会从题中获取解题的主要知识点是解题的关键,如第二问的解题关键是抓住“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”这句话.
(2)根据题意可知“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”,结合这句话从化合价的升高和降低来分析即可.
解答:解:(1)从图示可看出11--18号元素原子最外层电子数变化的趋势是:逐渐递增(或从1到8逐渐递增).
(2)乙同学的猜想不合理.
原因:若生成KOH和O2,则该反应中钾元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低.
故答案为:
(1)逐渐递增(或从1到8逐渐递增).
(2)乙;若生成KOH和O2,该反应中钾元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低.
点评:主要考查了化合价规律和原则,粒子结构示意图.要能准确的读图,认真阅读并会从题中获取解题的主要知识点是解题的关键,如第二问的解题关键是抓住“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”这句话.

练习册系列答案
相关题目



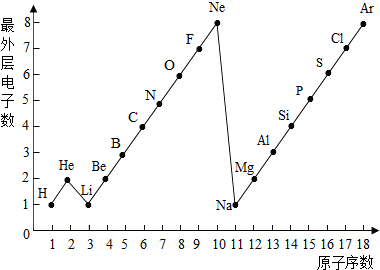 图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答: 图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答: