题目内容
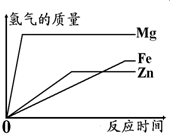
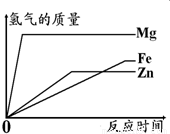
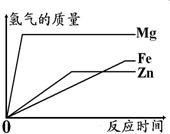 如图所示,为等质量的Mg、Zn、Fe与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析:
如图所示,为等质量的Mg、Zn、Fe与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析:
(1)等质量的三种金属与足量稀硫酸反应产生氢气的质量最少的金属是______;
(2)与相同浓度的稀硫酸反应时反应最快的金属是______;
(3)据图分析,实验室制氢气时应选择与稀硫酸反应的金属是______,理由是______.
解:(1)依据氢气的质量=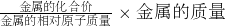 ,而Mg、Zn、Fe的相对原子质量分别是24、65、56,化合价均是+2,且质量相等,所以等质量的三种金属与足量稀硫酸反应产生氢气的质量最少的金属是Zn;
,而Mg、Zn、Fe的相对原子质量分别是24、65、56,化合价均是+2,且质量相等,所以等质量的三种金属与足量稀硫酸反应产生氢气的质量最少的金属是Zn;
(2)Mg、Zn、Fe三种金属的活动性顺序是Mg>Zn>Fe,所以与相同浓度的稀硫酸反应时反应最快的金属是镁,表现在图象中应该是斜率最大的物质;
(3)据图分析可知镁的反应速度很快,铁太慢,而锌的反应速度较适中,这样方便在制取气体是的收集操作;
故答案为:(1)Zn;(2)Mg;(3)Zn;其反应速率适中便于收集气体气体;
分析:(1)依据氢气的质量=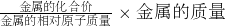 分析解答;
分析解答;
(2)依据三种金属的活动性对反应速度进行分析探讨即可;
(3)根据实验室制取氢气选择的药品要控制好反应的速度,从而方便收集分析解答即可;
点评:本题考查了金属活动性顺序的应用及实验室制取氢气的有关问题,完成此题,可以依据金属活动性顺序的意义以及实验室制取氢气的相关问题进行.
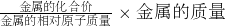 ,而Mg、Zn、Fe的相对原子质量分别是24、65、56,化合价均是+2,且质量相等,所以等质量的三种金属与足量稀硫酸反应产生氢气的质量最少的金属是Zn;
,而Mg、Zn、Fe的相对原子质量分别是24、65、56,化合价均是+2,且质量相等,所以等质量的三种金属与足量稀硫酸反应产生氢气的质量最少的金属是Zn;(2)Mg、Zn、Fe三种金属的活动性顺序是Mg>Zn>Fe,所以与相同浓度的稀硫酸反应时反应最快的金属是镁,表现在图象中应该是斜率最大的物质;
(3)据图分析可知镁的反应速度很快,铁太慢,而锌的反应速度较适中,这样方便在制取气体是的收集操作;
故答案为:(1)Zn;(2)Mg;(3)Zn;其反应速率适中便于收集气体气体;
分析:(1)依据氢气的质量=
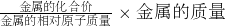 分析解答;
分析解答;(2)依据三种金属的活动性对反应速度进行分析探讨即可;
(3)根据实验室制取氢气选择的药品要控制好反应的速度,从而方便收集分析解答即可;
点评:本题考查了金属活动性顺序的应用及实验室制取氢气的有关问题,完成此题,可以依据金属活动性顺序的意义以及实验室制取氢气的相关问题进行.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
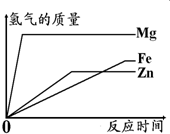 如图所示,为等质量的Mg、Zn、Fe与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析:
如图所示,为等质量的Mg、Zn、Fe与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析: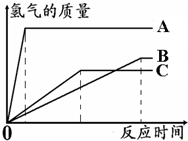 如图所示,为等质量的A、B、C与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析:
如图所示,为等质量的A、B、C与足量相同浓度的稀硫酸反应的关系.横坐标表示反应时间,纵坐标表示生成氢气的质量.据此分析: