题目内容
某溶液中溶质的质量分数为20%,则下列质量比关系不正确的是( )
分析:溶质的质量分数=
×100%,据此进行分析判断即可.
| 溶质质量 |
| 溶液质量 |
解答:解:溶质的质量分数=
×100%=20%,
=
,则溶质质量:溶剂质量:溶液质量=1:4:5.
A、溶质质量:溶剂质量=1:4,故选项说法正确.
B、溶质质量:溶液质量=1:5,故选项说法正确.
C、溶剂质量:溶液质量=4:5,故选项说法正确.
D、溶质质量:溶剂质量=1:4,故选项说法错误.
故选:D.
| 溶质质量 |
| 溶液质量 |
| 溶质质量 |
| 溶液质量 |
| 1 |
| 5 |
A、溶质质量:溶剂质量=1:4,故选项说法正确.
B、溶质质量:溶液质量=1:5,故选项说法正确.
C、溶剂质量:溶液质量=4:5,故选项说法正确.
D、溶质质量:溶剂质量=1:4,故选项说法错误.
故选:D.
点评:本题难度不大,掌握溶质的质量分数的概念、含义并能灵活运用即可正确解答本题.

练习册系列答案
相关题目
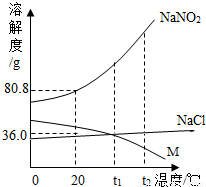
 (2009?连云港) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图所示,请根据图象和有关信息回答下列问题:
(2009?连云港) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图所示,请根据图象和有关信息回答下列问题: