题目内容
某化学实验小组在实验室中对一烧杯浑浊的河水进行了简单净化.
请回答下列有关问题:
(1)先向烧杯中加入适量明矾粉末,搅拌、静置一会,其目的是
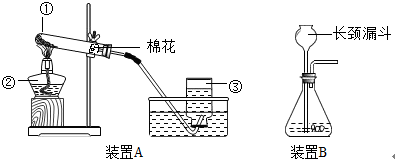
(2)再进行过滤液体.
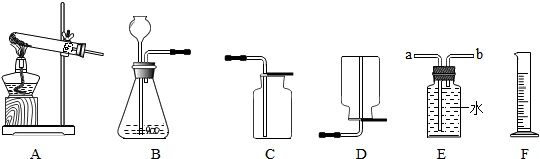
①过滤操作时用到的玻璃仪器有玻璃棒、漏斗、
②过滤时采取的下列操作中,错误的是
A.取一张圆形滤纸,对折两次,打开成圆锥形,放入漏斗
B.如果滤纸高于漏斗边缘,用剪刀剪去多余部分,使滤纸的边缘比漏斗口稍低
C.用少量水润湿滤纸,使滤纸紧贴漏斗内壁,滤纸层与漏斗壁间不留气泡
D.用玻璃棒轻轻搅动漏斗中的液体,以加快过滤
③若过滤的速度较慢,原因可能是
④若发现所得的滤液仍然很浑浊,请你分析可能的原因是
(3)然后用活性炭除去水中的异味.这是利用了活性炭的
(4)最后进行蒸馏.所得蒸馏水是
请回答下列有关问题:
(1)先向烧杯中加入适量明矾粉末,搅拌、静置一会,其目的是
吸附凝聚水中的悬浮杂质而沉降
吸附凝聚水中的悬浮杂质而沉降
(2)再进行过滤液体.
①过滤操作时用到的玻璃仪器有玻璃棒、漏斗、
烧杯
烧杯
.②过滤时采取的下列操作中,错误的是
D
D
(填标号).A.取一张圆形滤纸,对折两次,打开成圆锥形,放入漏斗
B.如果滤纸高于漏斗边缘,用剪刀剪去多余部分,使滤纸的边缘比漏斗口稍低
C.用少量水润湿滤纸,使滤纸紧贴漏斗内壁,滤纸层与漏斗壁间不留气泡
D.用玻璃棒轻轻搅动漏斗中的液体,以加快过滤
③若过滤的速度较慢,原因可能是
水样含杂质太多
水样含杂质太多
(写一条).④若发现所得的滤液仍然很浑浊,请你分析可能的原因是
滤纸破损
滤纸破损
(写一条).(3)然后用活性炭除去水中的异味.这是利用了活性炭的
吸附
吸附
作用.(4)最后进行蒸馏.所得蒸馏水是
软水
软水
(填“硬水”或“软水”),可以用肥皂水
肥皂水
来检验.分析:(1)根据加入明矾吸附凝聚水中的悬浮杂质而沉降进行解答;
(2)根据过滤的仪器以及注意事项进行解答;
(3)根据活性炭具有吸附性进行解答;
(4)根据蒸馏的原理进行解答.
(2)根据过滤的仪器以及注意事项进行解答;
(3)根据活性炭具有吸附性进行解答;
(4)根据蒸馏的原理进行解答.
解答:解:(1)先向烧杯中加入适量明矾粉末,搅拌、静置一会,其目的是:吸附凝聚水中的悬浮杂质而沉降;
(2)①过滤操作时用到的玻璃仪器有玻璃棒、漏斗、烧杯;
②用玻璃棒轻轻搅动漏斗中的液体,容易使滤纸破损,故错误;
③若过滤的速度较慢,原因可能是水样含杂质太多或没有先静置再过滤或滤纸层与漏斗壁间有气泡等;
④若发现所得的滤液仍然很浑浊,请你分析可能的原因是滤纸破损或滤液液面高于滤纸的边缘等;
(3)活性炭具有吸附性,能除去水中的异味;
(4)最后进行蒸馏.所得蒸馏水是软水,可以用肥皂水检验.
故答案为:(1)吸附凝聚水中的悬浮杂质而沉降;(2)①烧杯;②D;③水样含杂质太多;④滤纸破损;(3)吸附 (4)软水;肥皂水.
(2)①过滤操作时用到的玻璃仪器有玻璃棒、漏斗、烧杯;
②用玻璃棒轻轻搅动漏斗中的液体,容易使滤纸破损,故错误;
③若过滤的速度较慢,原因可能是水样含杂质太多或没有先静置再过滤或滤纸层与漏斗壁间有气泡等;
④若发现所得的滤液仍然很浑浊,请你分析可能的原因是滤纸破损或滤液液面高于滤纸的边缘等;
(3)活性炭具有吸附性,能除去水中的异味;
(4)最后进行蒸馏.所得蒸馏水是软水,可以用肥皂水检验.
故答案为:(1)吸附凝聚水中的悬浮杂质而沉降;(2)①烧杯;②D;③水样含杂质太多;④滤纸破损;(3)吸附 (4)软水;肥皂水.
点评:本考点考查了水的净化、硬水与软水的鉴别方法和实验方案的评价等,并且与生活实际相联系,考查了同学们根据学过的知识,解决实际问题的能力.要记忆活性炭的吸附作用和硬水与软水的鉴别方法,过滤操作中的指错和改错题,要注意语言描述的准确性.本考点主要出现在填空题和实验题中.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
某化学实验活动小组的同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。参与他们进行的探究活动:
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3; 猜想Ⅲ: 。
【实验与探究】
(1)分析:暴露在空气中的氢氧化钠会变质,变质原因是(用化学方程式表示)______________________
(2)实验如下:
|
实验操作步骤 |
实验现象 |
结论及解释 |
|
步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的_________。 |
实验过程中始终没有气泡产生。 |
则证明猜想 成立。 |
|
步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液。 |
实验过程中产生
|
则证明猜想Ⅱ或Ⅲ成立。此过程中发生反应的化学方程式为 _____________________ |
(3)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想_________成立;若酚酞不变红,则猜想______成立。
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈 性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是 。
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | ________ | 猜想a、c不成立,猜想b成立. |
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:
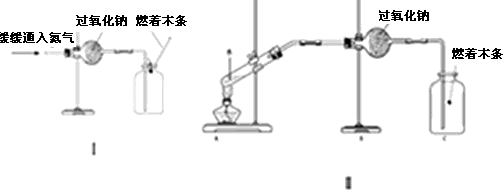
(1)实验现象及结论:观察到________现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是________.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式________.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. | A装置中观察到的现象有________, C装置中有气泡出现. | A装置中发生反应的化学方程式为________; C装置作用是________. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是________.请你回答如何改进该实验________.
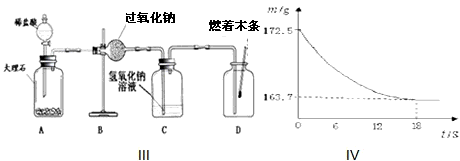
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:________.(写出计算过程,结果保留一位小数)
 (2013?克拉玛依二模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图)的溶液,他们对此产生了兴趣.
(2013?克拉玛依二模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图)的溶液,他们对此产生了兴趣.