题目内容
Ⅰ.实验室常用制取氧气的方法有:a、加热氯酸钾和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示.
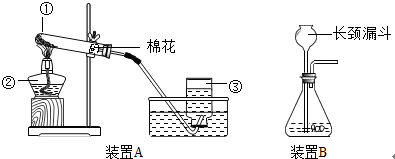
(1)写出图中指定仪器的名称:①
(2)用上图中的装置A来制取氧气的方法有
(3)利用装置A制氧气,棉花团的作用是
(4)实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:
(5)“绿色化学”是21世纪化学科学发展的重要方向之一.你认为在中学化学实验室中,a、b、c三种制取氧气的途径中,
Ⅱ.某实验小组的同学为了研究二氧化锰在过氧化氢分解反应中的作用,进行了以下探究:
【查阅资料】
①二氧化锰+盐酸(浓)
氯化锰+水+氯气,氯气为黄绿色气体,有刺激性气味.
②过氧化氢溶液为无色液体,在常温下能缓慢分解放出极少量氧气,在加热或有催化剂存在的条件下能快速分解出氧气.
【设计实验】
在常温下取一定量的过氧化氢溶液,放置一段时间能看到缓慢放出极少量气泡.加入4g二氧化锰粉末后,看到迅速放出大量气泡.不再产生气泡后,将反应后的物质过滤,将滤渣洗涤烘干,称得其质量为4g.
【分析与结论】
(1)分析实验现象和有关数据:根据二氧化锰能
(2)根据催化剂的概念,小刚认为以上实验还不足以证明二氧化锰是过氧化氢分解反应中的催化剂.他联系所查资料补做了以下实验,请你帮他完成实验报告:
小刚的实验说明,在过氧化氢分解反应中二氧化锰的
(3)在实验中,取用二氧化锰粉末用到的一种仪器是

(1)写出图中指定仪器的名称:①
试管
试管
;③集气瓶
集气瓶
.(2)用上图中的装置A来制取氧气的方法有
ab
ab
(填a、b或c).(3)利用装置A制氧气,棉花团的作用是
防止加热时高锰酸钾粉末进入导气管
防止加热时高锰酸钾粉末进入导气管
;在结束实验时要先将导管撤离出水面,再熄灭酒精灯,其目的是防止水倒吸,使试管炸裂
防止水倒吸,使试管炸裂
;利用装置B制氧气时,长颈漏斗的下端要插入液面以下,其目的是防止气体从下端管口逸出
防止气体从下端管口逸出
.(4)实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:
一有气泡就立即收集
一有气泡就立即收集
.(5)“绿色化学”是21世纪化学科学发展的重要方向之一.你认为在中学化学实验室中,a、b、c三种制取氧气的途径中,
c
c
途径更体现化学实验的绿色化追求.Ⅱ.某实验小组的同学为了研究二氧化锰在过氧化氢分解反应中的作用,进行了以下探究:
【查阅资料】
①二氧化锰+盐酸(浓)
| 加热 |
②过氧化氢溶液为无色液体,在常温下能缓慢分解放出极少量氧气,在加热或有催化剂存在的条件下能快速分解出氧气.
【设计实验】
在常温下取一定量的过氧化氢溶液,放置一段时间能看到缓慢放出极少量气泡.加入4g二氧化锰粉末后,看到迅速放出大量气泡.不再产生气泡后,将反应后的物质过滤,将滤渣洗涤烘干,称得其质量为4g.
【分析与结论】
(1)分析实验现象和有关数据:根据二氧化锰能
改变
改变
过氧化氢的分解速率,而本身的质量
质量
在反应前后没有改变,小强认为二氧化锰在过氧化氢分解反应中作催化剂.(2)根据催化剂的概念,小刚认为以上实验还不足以证明二氧化锰是过氧化氢分解反应中的催化剂.他联系所查资料补做了以下实验,请你帮他完成实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取实验后的滤渣放入试管中,加入适量浓盐酸并加热 | 滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味 滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味 |
滤渣仍为二氧化锰 |
化学性质
化学性质
不变.综合小强的分析和实验可以确定,二氧化锰是过氧化氢分解反应的催化剂.(3)在实验中,取用二氧化锰粉末用到的一种仪器是
药匙
药匙
.用二氧化锰作催化剂时,过氧化氢分解的文字表达式为过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
;二氧化锰在上述反应中分别作催化剂或反应物,它在某些反应中还可能是生成物,请写出一个它是生成物的文字表达式:| 二氧化锰 |
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
.| 加热 |
分析:试管是常用的反应容器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:一有气泡就立即收集;在a、b、c三种制取氧气的途径中,用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气的方法,节能环保,更体现化学实验的绿色化追求.根据二氧化锰和表格的信息可知:在过氧化氢分解反应中二氧化锰的质量不变;过氧化氢的分解速率变大,因此二氧化锰改变了分解速率;小刚的实验是:取实验后的滤渣放入试管中,加入适量浓盐酸并加热,现象是:滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味,因此滤渣滤渣仍为二氧化锰,说明在过氧化氢分解反应中二氧化锰的化学性质不变.取用二氧化锰粉末用到的仪器是药匙,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气.
解答:解:㈠(1)试管是常用的反应容器,集气瓶是收集气体的仪器,
故答案为:①试管③集气瓶
(2)装置A来制取氧气的方法有,加热氯酸钾和二氧化锰粉末制氧气,加热高锰酸钾固体制氧气,
故答案为:ab
(3)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
故答案为:防止加热时高锰酸钾粉末进入导气管;防止水倒吸,使试管炸裂;防止气体从下端管口逸出
(4)实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:一有气泡就立即收集;
故答案为:一有气泡就立即收集
(5)在a、b、c三种制取氧气的途径中,用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气的方法,节能环保,更体现化学实验的绿色化追求,
故答案为:c
㈡(1)根据二氧化锰和表格的信息可知:在过氧化氢分解反应中二氧化锰的质量不变;过氧化氢的分解速率变大,因此二氧化锰改变了分解速率;
故答案为:改变;质量
(2)小刚的实验是:取实验后的滤渣放入试管中,加入适量浓盐酸并加热,现象是:滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味,因此滤渣滤渣仍为二氧化锰,说明在过氧化氢分解反应中二氧化锰的化学性质不变;
故答案为:滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味;化学性质
(3)取用二氧化锰粉末用到的仪器是药匙,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气;
故答案为:药匙;过氧化氢
水+氧气;高锰酸钾
锰酸钾+二氧化锰+氧气;
故答案为:①试管③集气瓶
(2)装置A来制取氧气的方法有,加热氯酸钾和二氧化锰粉末制氧气,加热高锰酸钾固体制氧气,
故答案为:ab
(3)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
故答案为:防止加热时高锰酸钾粉末进入导气管;防止水倒吸,使试管炸裂;防止气体从下端管口逸出
(4)实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:一有气泡就立即收集;
故答案为:一有气泡就立即收集
(5)在a、b、c三种制取氧气的途径中,用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气的方法,节能环保,更体现化学实验的绿色化追求,
故答案为:c
㈡(1)根据二氧化锰和表格的信息可知:在过氧化氢分解反应中二氧化锰的质量不变;过氧化氢的分解速率变大,因此二氧化锰改变了分解速率;
故答案为:改变;质量
(2)小刚的实验是:取实验后的滤渣放入试管中,加入适量浓盐酸并加热,现象是:滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味,因此滤渣滤渣仍为二氧化锰,说明在过氧化氢分解反应中二氧化锰的化学性质不变;
故答案为:滤渣逐渐溶解,有黄绿色气体生成,同时能闻到刺激性气味;化学性质
(3)取用二氧化锰粉末用到的仪器是药匙,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气;
故答案为:药匙;过氧化氢
| 二氧化锰 |
| 加热 |
点评:本考点主要考查了仪器的名称、药品的取用、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和催化剂等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
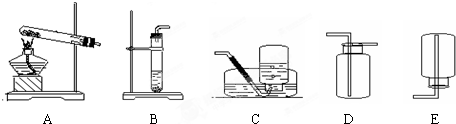
 实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示.
实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示. 实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示.
实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示.