��Ŀ����
����Ŀ����ѧ����ʵ��Ϊ������ѧ�ƣ����������ʵ��ش��й����⣺ 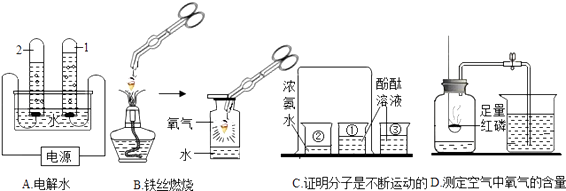
��1��Aʵ���Թ���1������������鷽�� �� ���ˮ��Ӧ�ķ��ű���ʽ �� ��ʵ�鳣��ˮ�м���һ������ϡ���������������Һ��Ŀ�� ��
��2��Bʵ��������״��˿��ĩ��ϵһ������������ �� д����˿ȼ�յķ��ű���ʽ ��
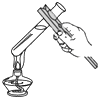
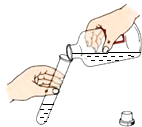
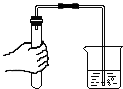
��3��Cʵ���й۲쵽�������� �� �ձ��۵������� ��
��4��Dʵ��˵�����������Լռ��������� �� Ϊȷ��ʵ��ɹ������ȱ�֤��װ�����������ã����װ�������Բ��ã�������O2�ĺ��������ƫ����ƫС�����䡱����д������ȼ�յķ��ű���ʽ ��
����������� ��
��ʵ��ǰ�н�ֹˮ�� ����ȴ���ٴ�ֹˮ�� ��ѡ�ý����ڵĿ�����
���𰸡�
��1���������ǵ�ľ�������Թ��У���ȼ��֤����������2H2O ![]() 2H2��+O2������ǿˮ�ĵ�����
2H2��+O2������ǿˮ�ĵ�����
��2����ȼ��˿�����ã�3Fe+2O2 ![]() Fe3O4
Fe3O4
��3�����ձ��е���Һ���ɫ����ʵ��Ķ����飨��֤��ʹ����Һ�����������ɢ���Һ�лӷ������ĵȣ�
��4��![]() ��ƫС��4P+5O2
��ƫС��4P+5O2 ![]() 2P2O5���٢�
2P2O5���٢�
���������⣺��1���ڵ��ˮʵ���У��ɹ۲쵽�������У���������������٣���ʹ�����ǵ�ľ����ȼ����������������࣬��ȼ�գ��������������ٵĶ�������������������Ƴ���������������������������������������������ͨ���۲�ͼ��֪��1�ܵ���������������ͨ���ô����ǵ�ľ�������Թ��ڣ�������ľ����ȼ��ˮ��ͨ�������¿ɷֽ�Ϊ���������������ˮ��Ӧ�ķ��ű���ʽ�ǣ�2H2O ![]() 2H2��+O2����ʵ��ʱ��ˮ�м���������ϡ������������ƣ�Ŀ���ǣ���ǿˮ�ĵ����ԣ���2��ͼ������״��˿��ĩ��ϵһ��������������ȼ��˿�����ã����������ڵ�ȼ��������������������������3��ͨ���ձ������ձ��۵ĶԱȷ��֣��ձ����еķ�̪��죬�ձ����еķ�̪����ɫ��˵���ǰ�ˮ�÷�̪�����������������÷�̪��죬����ˮ�ͷ�̪��û�л�ϣ��Ӷ�˵���������ڲ��ϵ��˶�����4������ȼ���Ǻ���������Ӧ���������������ף��÷�Ӧ�Ļ�ѧ����ʽΪ��4P+5O2
2H2��+O2����ʵ��ʱ��ˮ�м���������ϡ������������ƣ�Ŀ���ǣ���ǿˮ�ĵ����ԣ���2��ͼ������״��˿��ĩ��ϵһ��������������ȼ��˿�����ã����������ڵ�ȼ��������������������������3��ͨ���ձ������ձ��۵ĶԱȷ��֣��ձ����еķ�̪��죬�ձ����еķ�̪����ɫ��˵���ǰ�ˮ�÷�̪�����������������÷�̪��죬����ˮ�ͷ�̪��û�л�ϣ��Ӷ�˵���������ڲ��ϵ��˶�����4������ȼ���Ǻ���������Ӧ���������������ף��÷�Ӧ�Ļ�ѧ����ʽΪ��4P+5O2 ![]() 2P2O5����ʵ��˵��������Լռ������������֮һ�����װ�������Բ��ã��ᵼ���ⲿ�Ŀ��������Թܣ�ˮ���������Թ�С���Թ��ݻ���1/5��ʹ���ƫС��
2P2O5����ʵ��˵��������Լռ������������֮һ�����װ�������Բ��ã��ᵼ���ⲿ�Ŀ��������Թܣ�ˮ���������Թ�С���Թ��ݻ���1/5��ʹ���ƫС��
��ʵ��ɹ��Ĺؼ���װ�õ�������Ҫ�ã�ʵ��ǰ�н�ֹˮ�У�Ϊ�����ĵ����е�����������Ӧ�ù�����������ͬʱӦ�õ���ȴ���ٴ�ֹˮ�У����٢�����ȷ�ģ�
���Դ��ǣ���1���������ǵ�ľ�������Թ��У���ȼ��֤����������2H2O ![]() 2H2��+O2������ǿˮ�ĵ����ԣ���2����ȼ��˿�����ã�3Fe+2O2
2H2��+O2������ǿˮ�ĵ����ԣ���2����ȼ��˿�����ã�3Fe+2O2 ![]() Fe3O4����3�����ձ��е���Һ���ɫ�� ��ʵ��Ķ����飨��֤��ʹ����Һ�����������ɢ���Һ�лӷ������ĵȣ�����4��
Fe3O4����3�����ձ��е���Һ���ɫ�� ��ʵ��Ķ����飨��֤��ʹ����Һ�����������ɢ���Һ�лӷ������ĵȣ�����4�� ![]() ��ƫС��4P+5O2
��ƫС��4P+5O2 ![]() 2P2O5���٢ڣ�
2P2O5���٢ڣ�
�����㾫�������������Ļ�ѧ���ʺ͵��ˮʵ���ǽ����ĸ�������Ҫ֪�������Ļ�ѧ���ʣ����е����ʣ�֧��ȼ�գ��������������ˮ��ʵ�飺A.װ�èD�D�Dˮ�����B.��Դ����---ֱ����C.����������������Ƶ�Ŀ��----��ǿˮ�ĵ�����D.��ѧ��Ӧ��2H2O=== 2H2��+ O2����

 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�����Ŀ��ͬѧ�Ƿ���NaOH��Һ��NaHCO3��Һ��Ϻ����������������ʣ����������Ƿ����˻�ѧ��Ӧ������ʦ�İ����£�����ͨ������̽������֤��NaHCO3��Һ��NaOH��Һ�����˷�Ӧ�� 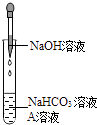
��1��ʵ��װ��
�ٲ������ϣ�NaHCO3+NaOH�TNa2CO3+H2O
����һ�����ʵ�����������NaHCO3��NaOH��Na2CO3������Һ��������ʵ�飬Ϊ���ʵ�鷽���ṩ�ο���
NaHCO3��Һ | NaOH��Һ | Na2CO3��Һ | |
����ϡ���� | ����� | �����Ա仯 | �������� |
�������ʯ��ˮ | ��Һ����� | �����Ա仯 | ����� |
����CaCl2��Һ | �����Ա仯 | ��Һ����� | ��Һ����� |
������Һ�����ڣ��� | ����ʯ��ˮ | ����ʯ��ˮ | ����ʯ��ˮ |
���е������Ϊ �� ������Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
��2��ʵ�����
��ʵ��1��֤����Ӧ������Na2CO3
ͬѧ��ѡ���ϱ�ʵ���е�ҩƷ���������ͼ��ʾʵ�飬����NaHCO3��Һ�м���A��Һ�������������ٵμ�NaOH��Һ����Һ����ǣ���A��Һ�� ��
��ͬѧ������ʵ�鲻����֤����Na2CO3���ɣ��������� �� Ϊ��֤����Na2CO3���ɣ���Ҫ�������еIJ����� ��
��ʵ��2��֤����Ӧ��NaHCO3������
ͬѧ�Dzο��ϱ��е�ʵ�飬�������һ��ʵ�飬��Ȼû�й۲쵽���Ե�ʵ����������֤����Ӧ�����ˣ���ʵ�鷽���� ��
��3��ʵ�鷴˼
ͨ��ʵ��1��ʵ��2˵��������û����������Ļ�ѧ��Ӧ�����Դ�������ͬ�ĽǶ�֤����Ӧ�ķ������������Ƕ��� ��