��Ŀ����
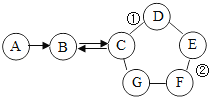
����Ŀ��ij��ѧ��ȤС����������װ�ý���O2��CO2��ʵ�����Ʒ����й����ʵ��о���
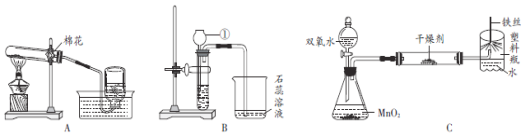
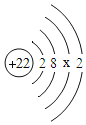
��1��д�����б�����������ƣ���_____��
��2����ͬѧ��Aװ����ȡO2����Ӧ�Ļ�ѧ����ʽΪ_____����O2�ռ���ֹͣ��ʵ�����ȷ������������_____����_____��
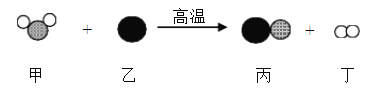
��3�����л�ѧ�仯�У���������Ϊ��Ӧ�����_____������ţ���
����Ȼ��ȼ�� �ڻ������� �۹������ �ܸ�������
��4����ͬѧ��Ũ����ʹ���ʯ��Bװ���з�Ӧ����ȡCO2���������й����ʡ��۲쵽�ձ�����ɫʯ����Һ��죬����һ�仯��Ϊ�����Ľ�����_____������ĸ����
A������CO2ֱ��ʹʯ����Һ���
B������CO2��ˮ��Ӧ����̼�ᣬ̼��ʹʯ����Һ���
C�ӷ������Ȼ�������ˮʹʯ����Һ���
��5��ͼC�ǡ���˿��������ȼ�ա�ʵ��ĸĽ�װ�ã�ʵ��ʱ����Һ©���Ļ�����һ��ʱ�����ȼ��˿�¶˻��ˣ���������ƿ�ڣ����������ܿ����Ϸ����۲쵽����������˿����ȼ�գ�_____��ʵ��Ľ�����ŵ���_____��дһ������
���𰸡�����©�� 2KMnO4![]() K2MnO4+MnO2+O2�� �ѵ����Ƴ�ˮ�� Ϩ��ƾ��� �� BC �������䣬���ɺ�ɫ���壬�ų��������� ������ǰ�Ʊ����ռ����������������㣨������ƿ���漯��ƿ����ֹ����ƿը�ѣ�����ȫ��װ�ü���������ȡ�������������֤��һ�壬ʵ����Ż����𰸺������ɣ�
K2MnO4+MnO2+O2�� �ѵ����Ƴ�ˮ�� Ϩ��ƾ��� �� BC �������䣬���ɺ�ɫ���壬�ų��������� ������ǰ�Ʊ����ռ����������������㣨������ƿ���漯��ƿ����ֹ����ƿը�ѣ�����ȫ��װ�ü���������ȡ�������������֤��һ�壬ʵ����Ż����𰸺������ɣ�
��������
��1������1�������dz���©����
��2��Aװ�����ø��������ȡ������װ�ã���������ڼ��ȵ������·�Ӧ��������ء��������̺���������Ӧ�ķ���ʽΪ��2KMnO4![]() K2MnO4+MnO2+O2������O2�ռ���ֹͣ��ʵ�����ȷ�����������Ƚ����ܴ�ˮ���Ƴ�����Ϩ��ƾ��ơ�
K2MnO4+MnO2+O2������O2�ռ���ֹͣ��ʵ�����ȷ�����������Ƚ����ܴ�ˮ���Ƴ�����Ϩ��ƾ��ơ�
��3������Ȼ��ȼ������Ȼ���������ڵ�ȼ�������·�Ӧ���ʲ��������⣻ �ڻ��������Ĺ�����������Ϊ��Ӧ��ʲ��������� �۹��������ֲ�����ն�����̼��ˮ���������������ǣ��ʷ������⣻ �ܸ�������������������ˮ��Ӧ���ʲ��������⡣��ѡ��.
��4��A��������CO2��ˮ��Ӧ���ɵ�̼����ʹʯ����Һ��죬��A����
B��������CO2��ˮ��Ӧ����̼�ᣬ̼��ʹʯ����Һ��죬��ȷ��
C��������лӷ��ԣ��ӷ������Ȼ�������ˮʹʯ����Һ��죬��ȷ����ѡBC��
��5�����������о���ȼ�գ��������䣬���ɺ�ɫ���壬�ų�������ʵ��Ľ�����ŵ���������ǰ�Ʊ����ռ����������������㣨������ƿ���漯��ƿ����ֹ����ƿը�ѣ�����ȫ��װ�ü���������ȡ�������������֤��һ�壬ʵ����Ż����𰸺������ɣ�

 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�����Ŀ����Һ���ճ������ũҵ�����������ڡ�
��1�����й�����Һ��˵����ȷ����_____��
A��Һһ������ɫ����
B��Һ���Ǿ�һ���ȶ��Ļ����
C�γ���Һ�����ʶ��ǹ���
Dͬ�����ʵı�����Һ���Ȳ�������ҺŨ�ȴ�
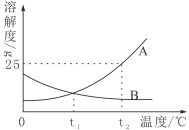
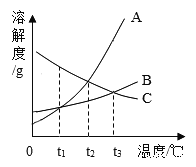
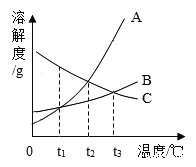
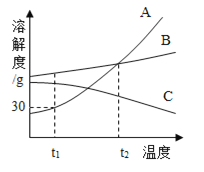
��2����ͼΪ�ס��ҡ����������ʵ��ܽ�����ߡ�
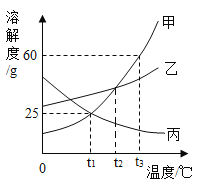
��t1��ʱ���ס��ҡ������������ܽ���ɴ�С��˳��Ϊ_____���á��������ݡ����������ܡ�������ʾ����ͬ��
��t2��ʱ�������ʵı�����Һ���µ�t1�棬������Һ���������������ɴ�С��˳��Ϊ_____��
����ͼ��֪�����ܽ�ȴ��ڱ����������ҵ��¶ȣ�T����ΧΪ_____��
����t3��ʱ80g�ı�����Һ���µ�t1�棬�������������Ϊ_____��
��3��С��ͬѧͨ��ʵ��̽���������ƺ��Ȼ����ܷ�����Ӧ���������ϵ�֪������ʵ��ܽ�����±���ʾ��
���� | �������� | �Ȼ��� | �Ȼ��� | �������� |
20��ʱ�ܽ��/g | 109 | 74.5 | 36 | 0.19 |
����С��ͬѧ��20%������������Һ��30%���Ȼ�����Һ��ϣ��۲쵽����������д���÷�Ӧ�Ļ�ѧ����ʽ_____��