题目内容
【题目】(11分)南京青奥会组委会承诺,保证2014年8月有一个“符合国际赛事标准的环境”。
(1)防止“雾霾围城”主要控制空气中 (填字母序号)的增加。
A. 二氧化碳 B. 一氧化碳 C. 二氧化硫 D. 可吸入颗粒物
(2)欲使燃料的充分燃烧通常考虑要有足够的空气和 ,化石燃料燃烧时排放出的 或其在空气中反应后的生成物溶于雨水,会形成酸雨。目前被认为是理想、清洁的高能燃料是 。
(3)下图是自然界碳、氧循环示意图。
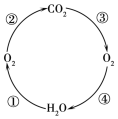
a. 图中③表示自然界中消耗二氧化碳的主要途径,其名称为 。
b. 按序号和规定的反应类型完成下列化学方程式
序号 | 反应类型 | 化学方程式 |
① | 分解反应 |
|
② | 化合反应 |
|
④ | 非基本反应类型 |
|
【答案】(1)D (2)要有与空气足够大的接触面积 二氧化硫、氮氧化合物; H2 (3)a.光合作用 b. ①2H2O![]() 2H2↑ + O2↑ ②C + O2
2H2↑ + O2↑ ②C + O2![]() CO2④ CH4 + 2O2
CO2④ CH4 + 2O2![]() CO2 + 2H2O(合理给分)
CO2 + 2H2O(合理给分)
【解析】
试题分析:(1)防止“雾霾围城”主要控制空气中D可吸入颗粒的增加;(2)欲使燃料的充分燃烧通常考虑要有足够的空气和)要有与空气足够大的接触面积,化石燃料燃烧时排放出的二氧化硫、氮氧化合物或其在空气中反应后的生成物溶于雨水,会形成酸雨。目前被认为是理想、清洁的高能燃料是氢气;(3)a. 图中③表示自然界中消耗二氧化碳的主要途径,其名称为光合作用,b. 按序号和规定的反应类型完成下列化学方程式①2H2O![]() 2H2↑ + O2↑ ②C + O2
2H2↑ + O2↑ ②C + O2![]() CO2④ CH4 + 2O2
CO2④ CH4 + 2O2![]() CO2 + 2H2O
CO2 + 2H2O

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】实验室区分下列各组物质的两种方法都合理的是( )
选项 | 待区分物质 | 方法一 | 方法二 |
A | 生铁和钢 | 用磁铁吸引 | 加稀盐酸 |
B | 浓硫酸和浓盐酸 | 尝味道 | 打开瓶盖闻气味 |
C | 氢氧化钠和硝酸铵 | 加入水中观察 | 观察颜色 |
D | 氧化铜和氧化铁 | 观察颜色 | 加入足量的稀盐酸 |
A. A B. B C. C D. D