题目内容
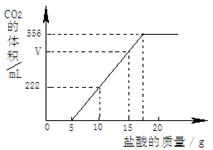
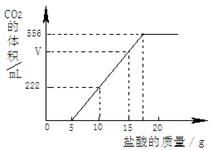
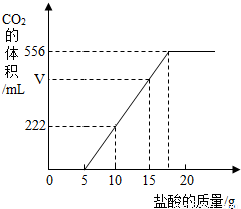
现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入27.6%的稀盐酸并不断振荡,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O。
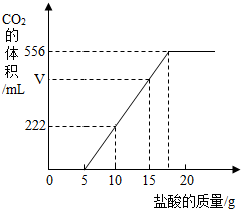
已知:实验测得产生的CO2的量与加入稀盐酸的数据如下图。
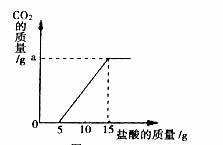
(1)当加入 g盐酸时,才开始产生CO2;
(2)原样品中Na2CO3的质量是多少?
(3)a的数值是 g。
(1) 5
(2)解:根据题意,当加入5g盐酸时,Na2CO3全部参加反应生成NaHCO3
设碳酸钠的质量为![]() g
g
NaCO3+HCl=NaHCO3+NaCl
106 36.5
![]() 5g×27.6%
5g×27.6%
106 :36.5=![]() :5g×27.6%
:5g×27.6%
![]()
(3)3.33

练习册系列答案
相关题目
 现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后才发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O.
现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后才发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O.