题目内容
【题目】如下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
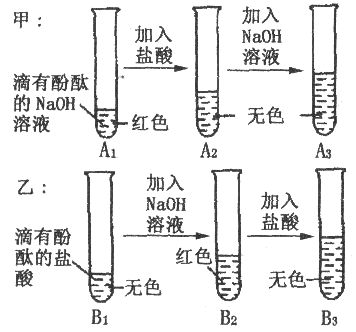
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据如图实验,请你与甲、乙同学一起完成下列探究:
探究环节 | 甲同学的探究 | 乙同学的探究 |
提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
实验验证 | (1)取少量A3,溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想_________(填“成立”或“不成立”); (2)你认为,在常温下A2溶液测出的pH应________(填“>”、“=”或“<”)7。 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变_________,据此,你认为乙同学的猜想_________(填“一”或“二”)成立。 |
交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是________________; (2)A3溶液未变红,你认为原因是A2溶液中___________较多,加入的NaOH溶液未将其完全中和; (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 | |
【答案】实验验证:甲同学的探究:(1)不成立
(2)<;乙同学的探究;浅绿色;二
交流反思:NaOH+HCl=NaCl+H2O;盐酸或氢离子
【解析】
试题分析:取少量A3,溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立,因为酚酞遇到碱会变红;在常温下A2溶液测出的pH应小于7,说明酸过量;取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变浅绿,据此,乙同学的猜想二成立,甲、乙同学的实验中,反应均涉及到的化学方程式是NaOH+HCl=NaCl+H2O;A3溶液未变红,你认为原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和,所以其溶液加入酚酞后变红。

 阅读快车系列答案
阅读快车系列答案【题目】(1)某化学兴趣小组利用下图装置探究制取气体的原理、方法.结合装置图,回答下列问题:
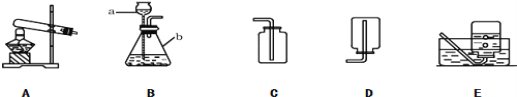
写出图中标号仪器的名称:a__________,b__________。
用高锰酸钾制取氧气时,可选用的发生装置是______________(填上图字母),可选用C装置收集氧气,其原因是_____________________,实验时应在试管口放一团棉花,其作用是__________________,用排水法收集氧气的合适时间是 __________________,写出该反应的表达式__________________.其反应类型为________________。
③实验室常用氯化铵固体与碱石灰固体共热来制取一种易溶于水密度比空气小的氨气(NH3),应选择的制取装置是___________、___________(填上图字母)。
(2)【发现问题】:小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现大量气泡产生.
①【提出问题】:小明联想到自己曾经用二氧化锰作过氧化氢的催化剂,他想,水泥块能否作过氧化氢分解的催化剂呢?于是他到建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究.
②【猜想】:水泥块能作过氧化氢分解的催化剂.
③【实验验证】:
实验步骤 | 实验现象 | 实验结论 | |
实验一 | _________________________. | 木条不复燃 | 常温下过氧化氢溶液分解很慢. |
实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | ____________________ |
④【结论】:水泥块能加快过氧化氢的分解速率,故水泥块是过氧化氢分解的催化剂.
⑤【讨论与反思】:小冰认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验:_______________________________;
实验步骤:Ⅰ准确称量水泥块质量;Ⅱ完成实验二;Ⅲ待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量;Ⅳ对比反应前后水泥块的质量;
⑥但老师指出:要证明小明的猜想,小冰的补充实验还是不足够,需要再补充一个探究实验: __________________________.