题目内容
(2010?海沧区质检)阅读下列微粒结构示意图及元素在周期表中的部分信息.回答问题:
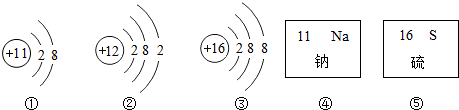
(1)①②③中,表示原子的是
(2)③的微粒是:
(3)①和③形成的化合物的化学式是

(1)①②③中,表示原子的是
②
②
(填序号,下同);表示阳离子的是①
①
;(2)③的微粒是:
S2-
S2-
(用化学用语表示);(3)①和③形成的化合物的化学式是
Na2S
Na2S
.分析:(1)依据原子中质子数等于核外电子数,质子数大于核外电子数为阳离子,质子数小于核外电子数为阴离子分析解答;
(2)依据该微粒所带的电荷数以及离子符号的书写要求分析解答;
(3)根据两者的化合价书写有关的化学式即可;
(2)依据该微粒所带的电荷数以及离子符号的书写要求分析解答;
(3)根据两者的化合价书写有关的化学式即可;
解答:解:(1)原子中质子数等于核外电子数,质子数大于核外电子数为阳离子,质子数小于核外电子数为阴离子,故可知②由于质子数=核外电子数=12可知是原子;而①由于质子数=11>核外电子数=10为阳离子;
(2)③的微粒质子数是16,核外电子数是18,所以是带两个单位负电荷的硫离子,符号为S2-;
(3)①钠元素③硫元素,其化合价分别是+1和-2,故形成的化合物的化学式是Na2S;
故答案为:(1)②;①;(2)S2-;(3)Na2S;
(2)③的微粒质子数是16,核外电子数是18,所以是带两个单位负电荷的硫离子,符号为S2-;
(3)①钠元素③硫元素,其化合价分别是+1和-2,故形成的化合物的化学式是Na2S;
故答案为:(1)②;①;(2)S2-;(3)Na2S;
点评:了解元素周期表的特点及其应用;了解原子结构示意图与离子结构示意图的特点是解题的关键所在;

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目

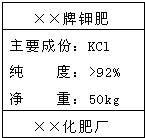 (2010?海沧区质检)“××牌”钾肥包装标签如图所示.某初三化学兴趣小组为检验该钾肥的纯度,进行了如下实验:称取3.2g该钾肥样品,加水完全溶解,加入适量AgNO3溶液至不再产生沉淀,过滤、洗涤、干燥,得到白色沉淀5.74g.
(2010?海沧区质检)“××牌”钾肥包装标签如图所示.某初三化学兴趣小组为检验该钾肥的纯度,进行了如下实验:称取3.2g该钾肥样品,加水完全溶解,加入适量AgNO3溶液至不再产生沉淀,过滤、洗涤、干燥,得到白色沉淀5.74g.