题目内容
【题目】柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
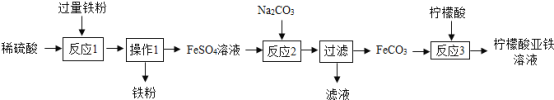
(1)写出反应1的化学方程式:__________;
(2)操作1的名称为__________;
(3)反应3中会有气体生成,该气体是_________;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为________;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水________g。
【答案】Fe + H2SO4 = Fe SO4 + H2↑ 过滤 CO2 7 : 9 1290
【解析】
(1)铁粉与稀硫酸反应生成硫酸亚铁和氢气,方程式Fe+H2SO4=FeSO4+H2↑;
(2)经过操作1,原来的反应液分成了液体和固体两部分,因此操作1为过滤;
(3)柠檬酸酸性强于碳酸,故柠檬酸与碳酸盐可反应生成二氧化碳气体,故气体为CO2;
(4)铁元素和碳元素质量比为其相对原子质量乘原子个数之比,即为56:6×12=7:9;
(5)100ml浓硫酸的质量为180g,其中硫酸的质量为180×98%=176.4g,需配置的稀硫酸质量分数为12%,则稀硫酸的总质量为硫酸质量除以质量分数=176.4/12%=1470g.则需要加水的质量为总质量-浓硫酸的质量=1470g-180g=1290g;
故答案为Fe+H2SO4=FeSO4+H2↑;过滤;CO2;7:9;1290。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定。已知,样品中的杂质不溶于水,且不与盐酸反应。测得数据如下表:
甲 | 乙 | 丙 | 丁 | |
所取石灰石样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
剩余固体的质量/g | 6.0 | m | 2.0 | n |
请回答:
(1)甲同学实验中碳酸钙_____剩余(有,或者没有)。
(2)石灰石样品中碳酸钙的质量分数是_____;(精确到0.1%)
(3)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克? _____(写出计算过程,计算结果精确到0.1 g)(可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40)
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。