题目内容
【题目】NaCl、KNO3、Ca(OH)2三种物质的溶解度曲线图如下图所示,下列说法正确的是( )
A.常温下,KNO3 , 的溶解度为85.5g
B.50%时,将50g NaCl溶解到100g水中,所得饱和溶液的浓度为37%
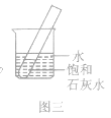
C.实验如图三,加热烧杯中的水至沸腾,试管中饱和石灰水变浑浊
D.用蒸发结晶的方法可除去混在KNO3 , 溶液中少量NaCl
【答案】C
【解析】A、50℃,KNO3的溶解度为85.5g,故选项A错误;B、50℃,NaCl的溶解度为37g,50gNaCl溶解到100g水中,形成饱和溶液的浓度为37g÷137g=27%,故选项B错误;C、氢氧化钙的溶解度随着温度的升高而减小,故选项C正确;D、KNO3的溶解度随温度的升高而增大,NaCl的溶解度受温度影响变化不大,应该用降温结晶的方法除去混在KNO3溶液中的少量NaCl。所以答案是C。
【考点精析】利用固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

 期末集结号系列答案
期末集结号系列答案【题目】某校探究小组欲利用周末完成以下两项探究任务:
(1)任务一:选择下图所示仪器组装一套实验室制取纯净、干燥CO:的装置,并验证性质。
①所选仪器的连接顺序为(填写仪器序号字母)。
②若用F装置收集CO2 , 气体应从(填a或b)端管口进入。
③将CO2通入到D装置中,可观察到的现象是。
④将CO2通入到盛有蒸馏水的洗气瓶中,一段时间后测得洗气瓶中溶液的pH7(填“>”、“=”、“<”)。
⑤将CO2通人到NaOH溶液中可以制取Na2CO3 , 请写出化学方程式。
(2)任务二:探究过氧碳酸钠的化学组成
【查阅资料】将Na2CO3和H2O2混合,在一定条件制取过氧碳酸钠,用作漂白洗涤剂。过氧碳酸钠(相对分子质量为122)是一种白色固体粉末,易溶于水,能与水反应生成Na2CO3和一种单质。
为了探究过氧碳酸钠的化学组成,同学们设计了以下实验,请完成表格内容。
序号 | 实验步骤 | 实验现象 | 实验结论或解释 |
① | 向盛有过氧碳酸钠固体的试管中加入适量水 | 固体溶解 | 过氧碳酸钠溶于水,能与水反应。 |
② | 向序号①的所得溶液中加入适量的MnO2粉末 | 有大量气泡产生 | MnO2的作用是。 |
③ | 将带火星的木条置于试管口 | 木条复燃 | 过氧碳酸钠与水反应生成的单质是(填化学式)。 |
④ | 取序号③试管中的上层清液加入CaCl2溶液 | 产生白色沉淀 | 反应的化学方程式为。 |
实验小结 | 推算过氧碳酸钠的化学式是。 | ||

