题目内容
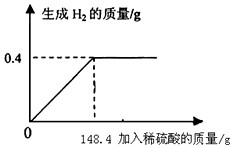
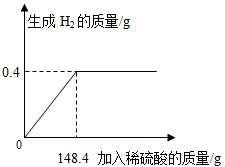 向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示.
向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示.求:
(1)样品中锌的质量.
(2)恰好完全反应时,所得溶液中溶质的质量分数.
分析:本题涉及的反应Zn+H2SO4═ZnSO4+H2↑,图象为充分反应所生成氢气的质量随加入稀硫酸质量的变化情况.根据曲线可确定加入148.4g稀硫酸时与锌恰好完全反应放出0.4g氢气,运用化学方程式由氢气质量计算参加反应锌的质量及生成硫酸锌的质量,最后由质量守恒定律计算反应后所得溶液质量,完成所得溶液中溶质的质量分数的计算.
解答:解:设样品中锌的质量为x,生成硫酸锌的质量为y.由图分析可知产生氢气0.4g.
Zn+H2SO4═ZnSO4+H2↑
65 161 2
x y 0.4g
=
x=13g
=
y=32.2g
恰好完全反应时,所得溶液中溶质的质量分数=
×100%=20%
答:(1)样品中锌的质量为13g;(2)所得硫酸锌溶液中溶质的质量分数为20%.
Zn+H2SO4═ZnSO4+H2↑
65 161 2
x y 0.4g
| 65 |
| x |
| 2 |
| 0.4g |
| 161 |
| y |
| 2 |
| 0.4g |
恰好完全反应时,所得溶液中溶质的质量分数=
| 32.2g |
| 13g+148.4g-0.4g |
答:(1)样品中锌的质量为13g;(2)所得硫酸锌溶液中溶质的质量分数为20%.
点评:解答此类问题的根本点在于对反应图象的曲线进行分析,曲线的折点表示此时恰好完全反应.

练习册系列答案
相关题目
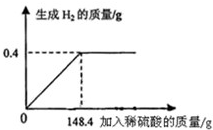 向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示,求:
向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示,求: