题目内容
【题目】过氧化钠(Na2O2)是淡黄色的粉末,在通常状况下能跟许多物质反应。如:2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2 2Na2O2+4HCl═4NaCl+2H2O+O2
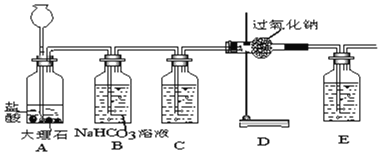
为了验证CO2跟Na2O2反应产生的气体是O2,某同学设计了如图所示的实验装置:
试回答下列问题:
(1)写出A中发生的化学反应的化学方程式_____。
(2)设计B、C的目的是净化CO2气体,其中B装置的作用是_____,C装置中的液体是_____,作用是_____,如果将B、C两瓶内所盛的液体互换,后果是_____ E装置的作用是_____。
(3)为了验证CO2和Na2O2反应产生的气体是O2,最后还要进行的实验操作是_____。
【答案】![]() 除去二氧化碳中混有的氯化氢气体 浓硫酸 除去水蒸气 水蒸气进入D中也生成氧气,影响实验结果 防止空气中水蒸气和二氧化碳进入D中 带火星木条放在E右侧的导管口
除去二氧化碳中混有的氯化氢气体 浓硫酸 除去水蒸气 水蒸气进入D中也生成氧气,影响实验结果 防止空气中水蒸气和二氧化碳进入D中 带火星木条放在E右侧的导管口
【解析】
(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:![]() ;
;
(2)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,浓硫酸具有吸水性,所以设计B、C的目的是净化CO2气体,其中B装置的作用是:除去二氧化碳中混有的氯化氢气体,C装置中的液体是:浓硫酸,作用是:除去水蒸气;
如果将B、C两瓶内所盛的液体互换,先通入浓硫酸中,可以出去水蒸气,再通入碳酸氢钠中,除去氯化氢气体,但是又引入水蒸气到二氧化碳气体中,所以将B、C两瓶内所盛的液体互换后果是:水蒸气进入D中也生成氧气,影响实验结果;E装置的作用是:防止空气中水蒸气和二氧化碳进入D中;
(3)氧气助燃性,所以为了验证CO2和Na2O2反应产生的气体是O2,最后还要进行的实验操作是:带火星木条放在E的右侧导管口。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案【题目】学习《海水“制碱”》的知识后,小明在实验室中进行了如下探究活动,请你和小明一起完成下面的实验探究活动。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
烧杯编号 | A | B | C | D |
水的质量/g | 100 | 100 | 100 | 100 |
加入 Na2CO3 的质量/g | 30 | 35 | 40 | 50 |
溶液的质量/g | 130 | 135 | 140 | 140 |
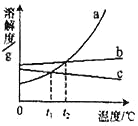
分析上述数据,烧杯编号为_________中的溶液是饱和溶液。
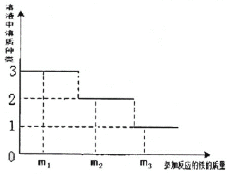
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
CaCl2 溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
沉淀的质量/g | 2 | 4 | m | 8 | 10 | 10 |
①m 的数值是 ______。
②计算纯碱样品中碳酸钠的质量分数______(写出计算过程,计算结果保留一位小数)。
③滴加氯化钙溶液过量的目的是______。
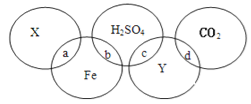
【题目】罗筝依同学为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。

(1)试管②中发生了化学反应,现象明显,该反应的化学方程式是_____。
(2)通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是_____。
(3)两支试管中的反应一段时间后,分别过滤,把滤液倒在烧杯中得到一种蓝色的混合液。黄一格同学由此认为试管①中Cu(NO)3溶液没有反应完,你认为他的结论正确吗?理由是_____。
同学们还想对混合液中的溶质成份进行探究:
(提出猜想)猜想一:_____;
猜想二:_____。
(设计实验)请选择其中一种猜想,并设计实验证明:
实验操作 | 实验现象 | 实验结果 |
取少量溶液于试管中,加入_____溶液 | _____。 | 猜想_____成立 |