题目内容
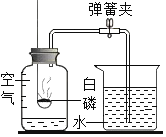
【题目】根据下列实验示意图,分析并计算:

查阅资料:98%浓硫酸的密度为1.84g/cm3,水的密度为1g/cm3
(1)实验1中所需水的体积是____________mL.
(2)实验2中NaOH溶液的溶质质量分数__________.(酚酞质量忽略不计)
【答案】165.6 16%
【解析】
(1)溶液稀释过程中溶质的质量不变;
(2)根据溶液总质量得到稀硫酸的质量,进而根据稀硫酸中溶质的质量和对应的化学方程式求算氢氧化钠溶液中溶质的质量分数。
(1)10mL即10cm3的浓硫酸的质量为1.84g/cm3×10cm3=18.4g,
设配制成的9.8%的稀硫酸的质量为x
18.4g×98%=9.8%x x=184g
则加入的水的质量=184g﹣18.4g=165.6g;由于水的密度为1g/cm3,所以体积为165.6cm3即165.6mL;
(2)由于反应中没有气体和沉淀产生,所以稀硫酸的质量为30g﹣10g=20g;
设:实验2中NaOH溶液的溶质质量分数为y
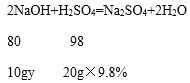
![]() y=16%
y=16%
答:(1)实验1中所需水的体积是 165.6mL。
(2)实验2中NaOH溶液的溶质质量分数为16%。

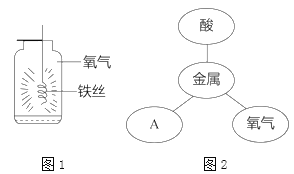
【题目】实验室有一瓶保管不当的试剂(如右图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小欣和小芳同学很感兴趣,决定对其成分进行探究.

(提出问题)这瓶试剂可能是什么溶液呢?
(讨论交流)根据受损标签的情况判断,这瓶试剂不可能是___________(填字母代号).
A.酸 B.碱 C.盐
(查阅资料)Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.测定室温(20℃)时,四种物质的溶解度的数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(作出猜想)小欣根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是NaHCO3,她的理由是__________________.
猜想1可能是NaOH溶液;猜想2可能是Na2CO3;猜想3可能是NaCl溶液.
(设计并实验)
a.小芳用胶头滴管吸取该溶液滴在pH试纸上.测得pH>7,则猜想__________不成立.
b.小欣为了检验该溶液是NaOH溶液还是Na2CO3溶液,她又进行了如下实验:
操作步骤 | 实验现象 | 结论及化学方程式 |
取样于试管中,滴加_________溶液 | 有气泡产生 | 该溶液是Na2CO3溶液,相关的化学方程式是_________. |
(反想交流)请你选择与小欣不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择__________溶液(填化学式).
【题目】阅读下面科普短文。
纯净的臭氧(O3)在常温下是天蓝色的气体,有难闻的鱼腥臭味,不稳定,易转化为氧气。它虽然是空气质量播报中提及的大气污染物,但臭氧层中的臭氧能吸收紫外线,保护地面生物不受伤害。而且近年来臭氧的应用发展较快,很受人们的重视。
生产中大量使用的臭氧通常由以下方法制得。
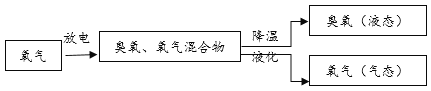
臭氧处理饮用水。早在19世纪中期的欧洲,臭氧已被用于饮用水处理。由于臭氧有强氧化性,可以与水中的有害化合物(如硫化铅)发生反应,处理效果好,不会产生异味。
臭氧做漂白剂。许多有机色素的分子遇臭氧后会被破坏,成为无色物质。因此,臭氧可作为漂白剂,用来漂白麻、棉、纸张等。实践证明,臭氧的漂白作用是氯气的15倍之多。
臭氧用于医用消毒。与传统的消毒剂氯气相比,臭氧有许多优点,如表1所示。
表1 臭氧和氯气的消毒情况对比
消毒效果 | 消毒所需时间(0.2 mg/L) | 二次污染 | 投资成本 (900 m3设备) | |
臭氧 | 可杀灭一切微生物,包括细菌、病毒、芽孢等 | < 5 min | 臭氧很快转化为氧气,无二次污染,高效环保 | 约45万元 |
氯气 | 能杀灭除芽孢以外的大多数微生物,对病毒作用弱 | > 30 min | 刺激皮肤,有难闻气味,对人体有害,有二次污染、残留,用后需大量水冲洗 | 约3~4万元 |
依据文章内容回答下列问题。
(1)说出氧气(O2)和臭氧(O3)的共同点______(至少一点)。
(2)臭氧处理饮用水时,利用了臭氧的______(填“物理”或“化学”)性质。
(3)臭氧转化为氧气的微观示意图如下,请在空白方框中补全相应微粒的图示。____
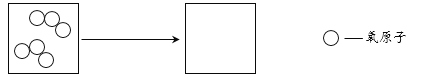
(4)依据表1信息,为了快速杀灭病毒,应选择的消毒剂是______。
(5)下列关于臭氧的说法中,正确的是______(填序号)。
A.臭氧的漂白作用比氯气强
B.由氧气制得臭氧的过程中,既有物理变化也有化学变化
C.臭氧在生产生活中有很多用途,对人类有益无害
D.臭氧稳定性差,不利于储存,其应用可能会受到限制