题目内容
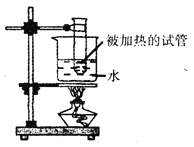
【题目】空气、水是人类赖以生存的自然资源。
(1)测定空气中氧气体积分数的实验装置如下图所示。在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内过量的红磷后,立即伸入瓶中并把塞子塞紧。
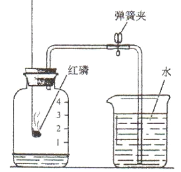
①写出红磷在空气中燃烧的文字表达式或化学方程式:_____
②红磷熄灭后,集气瓶内剩下的气体主要是_____,该气体_____(填“支持”或“不支持”)燃烧。
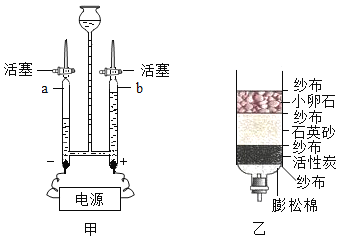
(2)如下图所示,在一个具有刻度和可以左右滑动的活塞的玻璃容器里放入白磷(足量,白磷着火点为40℃),活塞左端管内密封有空气,将玻璃容器固定在盛有80℃热水的烧杯上,进行实验,请回答。
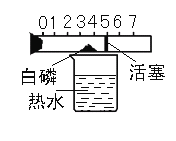
①整个实验过程中可观察到玻璃管内活塞的运动情况是:_____移动。
②实验结束后,恢复到常温后,活塞停在约刻度_____处(填数字)。
【答案】红磷+氧气![]() 五氧化二磷(或
五氧化二磷(或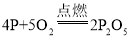 ) 氮气 不支持 先向右移动,后向左 4
) 氮气 不支持 先向右移动,后向左 4
【解析】
(1)①红磷在空气中燃烧生成五氧化二磷,反应的文字表达式为:红磷+氧气![]() 五氧化二磷(或
五氧化二磷(或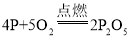 );
);
②空气的主要成分是氮气和氧气,红磷燃烧消耗氧气。故红磷熄灭后,集气瓶内剩下的气体主要是氮气,该气体不支持燃烧;
(2)①白磷燃烧放出大量的热,气体受热膨胀,活塞向右移动,白磷燃烧结束后,冷却到室温,消耗完玻璃容器里的氧气,玻璃容器里气体减少,压强降低,活塞向左移动。故整个实验过程中可观察到玻璃管内活塞的运动情况是:先向右移动,后向左移动;
②足量的白磷消耗完玻璃容器里的氧气,由于氧气约占空气体积的五分之一,故活塞停在约刻度4处。

 全程金卷系列答案
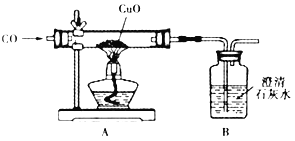
全程金卷系列答案【题目】某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
(1)从安全环保的角度考虑,上述实验需要改进的是_____。
(2)装置A中发生反应的化学方程式为_____。
(3)同学们通过查阅资料得知:氧化亚铜(Cu2O)和铜均为红色固体,且Cu2O能和稀硫酸反应,反应的化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O.他们对反应后玻璃管中的红色固体进行如下探究:
(提出问题)反应后生成的红色固体成分是什么?
(作出猜想)猜想一:红色固体只有Cu
猜想二:红色固体只有Cu2O
猜想三:红色固体可能含有_____。
(实验探究)设计如下实验方案
实验操作 | 现象 | 结论 |
取少量红色固体于试管中,加入过量的稀硫酸。 | _____ | 红色固体含有Cu2O |
(思考与分析)甲同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是_____。为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,然后过滤、洗涤、干燥、称量,得到ng固体。当n>_____(含m的代数式)时,可以得出猜想三的结论正确。