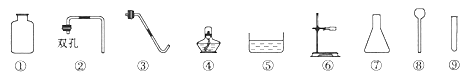
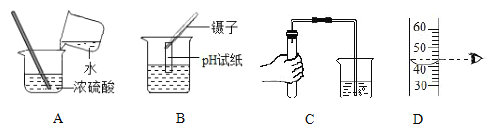
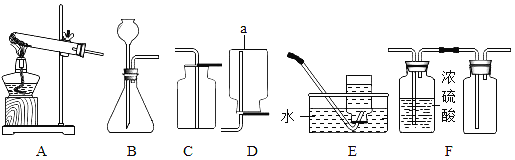
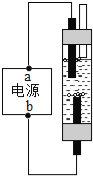
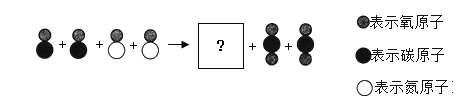
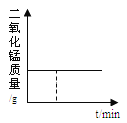
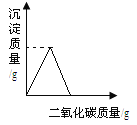
题目内容
【题目】某研究性学习小组通过查阅资料获知以下信息:将二氧化碳气体慢 慢地通入一定量的氢氧化钠溶液中,在溶液中先后发生以下两个化学反应:
2NaOH +CO2=Na2CO3+H2O (先发生反应) Na2CO3+CO2+H2O=2NaHCO3(后发生反应)
同学们开展了下列探究活动:
【提出问题】 将二氧化碳气体慢慢地通入一定量的氢氧化钠溶液中, 反应后所得溶液中溶质的成分有哪些?
【猜想假设】Ⅰ.NaHCO3 和 Na2CO3; Ⅱ.只有 NaHCO3 ;
Ⅲ.__________________ ; Ⅳ._____________________ .
小资料:Na2CO3+HCl=NaHCO3+NaCl NaHCO3+HCl= NaCl+H2O+CO 2↑
NaHCO3+NaOH=Na2CO3+H2O
【实验探究】 学习小组的同学将二氧化碳气体慢慢地通入一定量的某氢氧化钠溶液中,对溶液的成分进行探究后发现猜想Ⅲ、Ⅳ是不成立的。
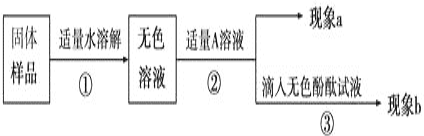
为了进一步验证剩下的猜想,按下列流程进行实验并测出相关数据:

【获得结论】 根据上述信息, 分析反应后所得溶液中溶质的成分为__________,X溶液为____________,所得溶液A的成分为 _____________________
【答案】 NaOH和 Na2CO3 Na2CO3 NaHCO3 和 Na2CO3 NaOH溶液 NaOH和Na2CO3
【解析】【猜想假设】如果氢氧化钠过量,则溶液中的溶质是没参与反应的NaOH和生成的Na2CO3,如果恰好反应,溶质是Na2CO3【实验探究】因为NaHCO3+NaOH=Na2CO3+H2O,所以加入的过量X溶液是NaOH溶液,BaCl2 + Na2CO3 == BaCO3↓+ 2NaCl,设生成19.7gBaCO3反应掉碳酸钠的质量为y。
Na2CO3 ----BaCO3
106 197
y 19.7g
![]() =
=![]() ,解得y=10.6g
,解得y=10.6g
设生成19.7gBaCO3,反应掉碳酸氢钠的质量为w
NaHCO3-----BaCO3
84 197
w 19.7g
![]() =
=![]() ,解得w=8.4g ,8.4g<10g<10.6g,所以反应后所得溶液中溶质的成分为NaHCO3和Na2CO3,由于加入过量的NaOH溶液,因此溶液A的成分为过量的NaOH和生成的Na2CO3。
,解得w=8.4g ,8.4g<10g<10.6g,所以反应后所得溶液中溶质的成分为NaHCO3和Na2CO3,由于加入过量的NaOH溶液,因此溶液A的成分为过量的NaOH和生成的Na2CO3。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案