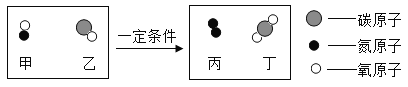
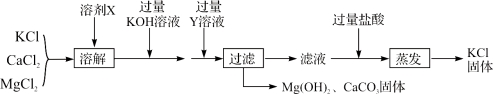
题目内容
【题目】在某过氧化氢溶液中,氢元素和氧元素的质量比为2:17,现向38g该溶液中加入1g二氧化锰,充分反应后生成氧气的质量为
A. 17gB. 3.2gC. 8.4gD. 2g
【答案】D
【解析】
过氧化氢溶液有H2O和H2O2,根据氢氧元素质量比可以算出过氧化氢的含量,然后根据氢元素的质量守恒就可以算出生成氧气的质量。
解:某H2O2溶液中H、O的质量比为2:17;则:38g双氧水溶液中氢元素质量为:38g×![]() =4g;根据过氧化氢分解的化学方程式可以知道,过氧化氢完全反应后生成水和氧气,该过程中氢元素的质量没有改变;所以反应后水的质量为:4g÷
=4g;根据过氧化氢分解的化学方程式可以知道,过氧化氢完全反应后生成水和氧气,该过程中氢元素的质量没有改变;所以反应后水的质量为:4g÷![]() ×100%=36g,所以根据质量守恒定律可以知道生成氧气的质量为 38g-36g=2g。
×100%=36g,所以根据质量守恒定律可以知道生成氧气的质量为 38g-36g=2g。
故选D。

 互动英语系列答案
互动英语系列答案【题目】某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
(1)从安全环保的角度考虑,上述实验需要改进的是_____。
(2)装置A中发生反应的化学方程式为_____。
(3)同学们通过查阅资料得知:氧化亚铜(Cu2O)和铜均为红色固体,且Cu2O能和稀硫酸反应,反应的化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O.他们对反应后玻璃管中的红色固体进行如下探究:
(提出问题)反应后生成的红色固体成分是什么?
(作出猜想)猜想一:红色固体只有Cu
猜想二:红色固体只有Cu2O
猜想三:红色固体可能含有_____。
(实验探究)设计如下实验方案
实验操作 | 现象 | 结论 |
取少量红色固体于试管中,加入过量的稀硫酸。 | _____ | 红色固体含有Cu2O |
(思考与分析)甲同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是_____。为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,然后过滤、洗涤、干燥、称量,得到ng固体。当n>_____(含m的代数式)时,可以得出猜想三的结论正确。

【题目】在探究氢氧化钙与稀盐酸中和反应实验时,忘记了滴加酚酞溶液,无法判断反应进行到何种程度,同学们决定对反应后溶液中溶质的成分进行探究。
请写出该反应的化学方程式。_____
(提出问题)反应后溶液中的溶质是什么?
(做出猜想)猜想一:CaCl2 和 Ca(OH)2 猜想二:CaCl2 和 HCl猜想三:_____
(设计方案)
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞试液 | _____。 | 猜想一不正确 |
②另取少量反应后的溶液于试管中,加入_____。 | _____。 | 猜想二不正确 |
(拓展与应用)将稀盐酸逐滴匀速加入一定量的稀氢氧化钙溶液中,用数字化仪器对反应过程中溶液的温度、pH 进行实时测定,得到的曲线如图 1、图2所示。

由图 1、图2知,稀盐酸与稀氢氧化钙溶液已发生中和反应的判断依据是_____。