题目内容
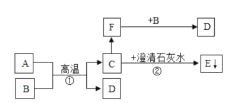
【题目】利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制取氧气的流程图:
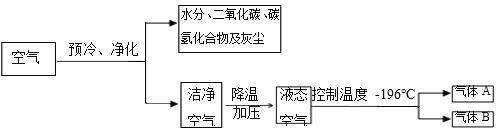
资料:氮气的沸点是-196°C,氧气的沸点是-183°C
(1)气体A在空气中的体积分数是_____。
(2)空气变为液态空气的过程,气体分子之间的间隙在_____(填“增大”或“减小”)。
(3)液态B是_____(填化学式)。
(4)请提出一条保护空气的措施_____。
【答案】78% 减小 O2 绿色出行等
【解析】
(1)空气中各成分的含量按体积分数计算,氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳占0.03%,氮气的沸点是-196°C,氧气的沸点是-183°C,-196°C时,先蒸发出来的气体A是氮气,在空气中的体积分数是78%;
(2)空气变为液态空气的过程,总体积减小,气体分子之间的间隙在减小;
(3)液态B主要是液态氧气,化学式为:O2;
(4)保护空气的措施:少开私家车,工厂废气处理达标后再排放,不露天焚烧垃圾等废弃物等。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是NaCl和KNO3物质在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
温度(℃) | 10 | 20 | 30 | 40 | 60 |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 |
(1)20℃时,NaCl的溶解度是_____g/100g水;
(2)以上两种物质溶解度变化受温度影响较小的是_____(选填“NaCl”或“KNO3”);
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为_____g;
(4)为了将混有少量NaCl杂质的KNO3的饱和溶液提纯,可通过_____方法获得较纯净的KNO3晶体;
(5)40℃时,将NaCl和KNO3的饱和溶液各100g降温到20℃,对剩余溶液描述正确的是_____。
A 溶质的质量分数:NaCl<KNO3
B 析出固体的质量:NaCl>KNO3
C NaCl和KNO3都是饱和溶液
D 溶剂的质量:NaCl>KNO3