题目内容
(2011?梧州)含碳元素质量相同的一氧化碳和二氧化碳的质量比为( )
分析:先分别算出一氧化碳和二氧化碳的碳元素的质量分数,然后假定碳元素的质量是M,最后分别计算一氧化碳和二氧化碳的质量.
也可根据物质的质量比是相对分子质量乘以分子个数之比
也可根据物质的质量比是相对分子质量乘以分子个数之比
解答:解:解法一:假定碳元素的质量是M克.
一氧化碳中碳元素的质量分数=
×100%,则一氧化碳的质量=M÷
═
.
二氧化碳中碳元素的质量分数=
×100%,则二氧化碳的质量=M÷
═
.
∴一氧化碳与二氧化碳的质量比为
:
=7:11.
故选C.
解法二:含相同质量碳元素其一氧化碳和二氧化碳的分子个数比为1:1
故一氧化碳和二氧化碳的质量比为:(28×1):(44×1)═7:11
故选C.
一氧化碳中碳元素的质量分数=
| 12 |
| 28 |
| 12 |
| 28 |
| 7M |
| 3 |
二氧化碳中碳元素的质量分数=
| 12 |
| 44 |
| 12 |
| 44 |
| 11M |
| 3 |
∴一氧化碳与二氧化碳的质量比为
| 7M |
| 3 |
| 11M |
| 3 |
故选C.
解法二:含相同质量碳元素其一氧化碳和二氧化碳的分子个数比为1:1
故一氧化碳和二氧化碳的质量比为:(28×1):(44×1)═7:11
故选C.
点评:就选择题来说,我们可以假定碳元素的质量为1克,这样简单、方便.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
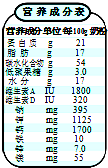 (2011?梧州模拟)如图是某品牌奶粉的营养成分表,由表中可知
(2011?梧州模拟)如图是某品牌奶粉的营养成分表,由表中可知