题目内容
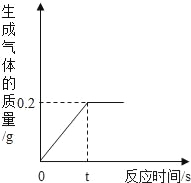
【题目】 化学兴趣小组的同学取10g铜锌合金样品于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:
(1)样品中锌的质量为_____ g。
(2)反应后,所得溶液中溶质的质量分数为多少________?
【答案】6.5 16.1%
【解析】
由图中数据可知生成氢气的质量,根据氢气的质量可以计算锌和生成硫酸锌的质量,进一步可以计算溶液中硫酸锌的质量分数。
(1)由图可知完全反应后生成氢气的质量为0.2g,
设锌的质量为x,生成硫酸锌的质量为y
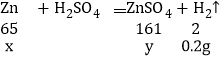
![]() ;解得:x=6.5g y=16.1g;故填:6.5
;解得:x=6.5g y=16.1g;故填:6.5
(2)反应后所得溶液中溶质的质量分数为:![]()
答:反应后,所得溶液中溶质的质量分数为16.1%。故填:16.1%

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
【题目】向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用如图曲线表示的是( )
序号 | 甲 | 乙 |
① | HNO3和Mg(NO3)2的混合溶液 | KOH溶液 |
② | Ag﹣Zn合金 | 稀H2SO4 |
③ | 久置空气中的铝片 | 稀盐酸 |
④ | 含有Na2CO3的NaOH溶液 | 稀HNO3 |
⑤ | HCl和H2SO4的混合酸 | Ba(NO3)2溶液 |
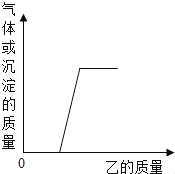
A. ②⑤ B. ①③④ C. ①②④ D. ①③⑤