题目内容
【题目】中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。某大型工厂利用此原理处理含硫酸铜的废液回收金属铜时,向100kg的废液中加入足量的铁粉,得到金属铜6.4kg。
(1)计算废液中硫酸铜的质量分数是多少?______
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有_______(写一条)。
【答案】16% 防止金属锈蚀(或寻找金属替代品;有计划合理开采)(答案合理即得分)
【解析】
硫酸铜和铁反应生成硫酸亚铁和铜。
(1)设废液中硫酸铜的质量为x
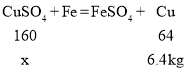
![]()
![]()
废液中硫酸铜的质量分数为![]()
答:废液中含硫酸铜的质量分数为16%。
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有防止金属锈蚀(或寻找金属替代品;有计划合理开采)。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 点燃 |
B | 鉴别石灰水和 | 通入二氧化碳气体 |
C | 检验一瓶O2是否收集满 | 将带火星的木条伸入瓶中 |
D | 比较 | 将 |
A.AB.BC.CD.D
【题目】某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题。
部分钙、镁化合物溶解性表(20℃) | |||
| OH- | CO32- | HCO3- |
Ca2+ | 微溶 | 不溶 | 可溶 |
Mg2+ | 不溶 | 微溶 | 可溶 |
(查阅资料) 天然水中含有![]() 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
(提出猜想)水垢的主要成分一定有CaCO3和_____(填化学式),可能含有Ca(OH)2和_____。
(设计方案)
实验1 确定水垢中是否含有 Ca(OH)2
实验步骤 | 现象 | 结论 |
在少量研体的水垢中,加入适量的蒸馏水充分搅拌、过滤,在滤液中加入Na2CO3溶液 | ___________ | 一定不含Ca(OH)2 |
实验2:确定水垢中是否含MgCO3
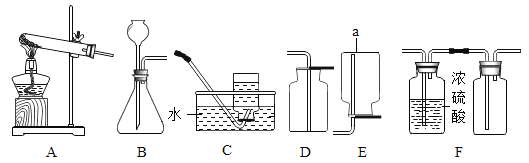
利用下列实验装置,完成实验2探究。

其主要实验步骤如下:称量D、E装置总质量为200.0g,按上图组装后,将2.5g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为201.25g(碱石灰主要分为CaO和NaOH,不考虑装置内空气对实验的影响)。
(实验讨论)
(1)反应结束后打开止水夹K,缓缓鼓入空气的目的是___________。A、B装置之间__________设置干燥装置。(填“要”或“不要”)其理由是____________。
(2)装置B盛放稀盐酸的仪器作用是_________________。
(3)装置B中生成气体的反应的化学方程式为_______________。
(4)装置B中生成CO2的质量为_________g,通过计算说明水垢中_________含MgCO3(填字母)。
A 一定不 B 一定 C 可能 D 无法确定
计算过程(已知CaCO3相对分子质量为100。MgCO3相对分子质量为84):___________
实验3:确定水垢中是否有Mg(OH)2
(5)另取质量为1.25g水垢,加入3.65%稀盐酸与之反应,测得消耗稀盐酸mg,结合上述实验,判断当m的值满足____________条件时,水垢中一定含有Mg(OH)2。写出计算过程。