题目内容
(7分)下图为用镀锌铁片制成的日常用品。镀锌铁是指通过镀锌工艺在铁皮上进行镀锌而制成的一种产品,热镀锌产品广泛用于建筑、家电、车船、容器制造业、机电业等,几乎涉及到衣食住行各个领域。

为测定铁片镀锌层的厚度实验过程如下。
【实验步骤】
⑴ 剪取一片镀锌铁片,量得长度=2.0cm,宽度=1.9cm。
⑵ 用电子天平称量质量0.857g。
⑶ 实验中需要溶质质量分数为10%的稀盐酸200mL(密度=1.05g/mL),需要量取溶质质量分数为37%的浓盐酸(密度=1.18g/mL) mL(保留至小数点后1位),然后稀释。
⑷ 将镀锌铁片放入溶质质量分数为10%盐酸中。当观察到 ,可以判断镀锌层恰好反应。
⑸ 将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g。
【计算结果】
⑴ 铁片镀锌层的质量有 g。
⑵ 已知锌的密度7.1g/cm3,计算出铁片镀锌层厚度mm(保留至小数点后2位)。
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间 。(填“偏长”、“偏短”)
【实验改进】
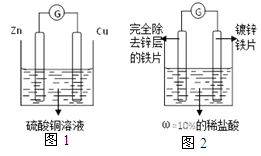
资料卡片:如图1所示,两种金属活动性不同的金属放入酸碱盐溶液中,会有电子的流动,从而产生电流。
将上述实验改进成如图2的装置,当观察到 ,此时锌层恰好反应。

为测定铁片镀锌层的厚度实验过程如下。
【实验步骤】
⑴ 剪取一片镀锌铁片,量得长度=2.0cm,宽度=1.9cm。
⑵ 用电子天平称量质量0.857g。
⑶ 实验中需要溶质质量分数为10%的稀盐酸200mL(密度=1.05g/mL),需要量取溶质质量分数为37%的浓盐酸(密度=1.18g/mL) mL(保留至小数点后1位),然后稀释。
⑷ 将镀锌铁片放入溶质质量分数为10%盐酸中。当观察到 ,可以判断镀锌层恰好反应。
⑸ 将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g。
【计算结果】
⑴ 铁片镀锌层的质量有 g。
⑵ 已知锌的密度7.1g/cm3,计算出铁片镀锌层厚度mm(保留至小数点后2位)。
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间 。(填“偏长”、“偏短”)
【实验改进】
资料卡片:如图1所示,两种金属活动性不同的金属放入酸碱盐溶液中,会有电子的流动,从而产生电流。
将上述实验改进成如图2的装置,当观察到 ,此时锌层恰好反应。

【实验步骤】(3)48.1mL (4)气泡产生的速率突然减慢
【计算结果】(1)0.02g (2)0.37mm
【实验反思】偏长
【实验改进】电流计指针指向“0”
【计算结果】(1)0.02g (2)0.37mm
【实验反思】偏长
【实验改进】电流计指针指向“0”
试题分析:【实验步骤】(3)这是一个溶液配制的稀释问题,抓住稀释过程中溶质的质量不变列等式,可设需要浓盐酸的体积为V,则200ml×1.05g/ml×10%=V×1.18g/ml×37%,解得V=48.1ml
(4)根据锌的活动性比铁强,与盐酸反应时,锌的反应速率更快,所以将镀锌铁片放入溶质质量分数为10%盐酸中。当观察到:气泡产生的速率突然减慢,可以判断镀锌层恰好反应
【计算结果】(1)反应开始前用电子天平称量质量0.857g,反应结束后将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g,所以铁片镀锌层的质量=0.857g-0.837g=0.02g
(2)根据密度的公式:V="0.02g/7.1g/" cm3="0.0028" cm3,再根据体积的计算公式:计算出铁片镀锌层厚度0.37mm
【实验反思】实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间偏长
【实验改进】根据两种金属活动性不同的金属放入酸碱盐溶液中,会有电子的流动,从而产生电流所以将上述实验改进成如图2的装置,当观察到:电流计指针指向“0”,此时锌层恰好反应

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目