题目内容
【题目】学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙。请你和同学们一起完成探究过程:
(设计实验)
实 验 操 作 | 实 验 现 象 |
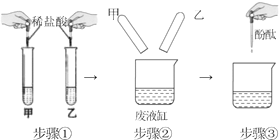
| 步骤①:甲溶液中观察到现象A, 乙溶液中无明显现象 步骤②:底部有白色沉淀 步骤③:上层为无色透明的溶液 |
(科学探究)
(1)碳酸钠属于____(选填“酸”、“碱”、“盐”)类物质,其水溶液呈碱性。写出甲乙两种物质混合发生反应的化学方程式:_____。
(2)现象A是有气泡产生,则甲溶液是____;产生该现象的化学方程式是___;该反应属于基本反应类型中的____。
(3)根据步骤③实验现象则上层溶液中一定含有的溶质是____(酸碱指示剂除外),可能含有的溶质是______。
【答案】盐 ![]() 碳酸钠 Na2CO3+2HCl═2NaCl+H2O+CO2↑ 复分解反应 氯化钠 氯化钙
碳酸钠 Na2CO3+2HCl═2NaCl+H2O+CO2↑ 复分解反应 氯化钠 氯化钙
【解析】
(1)碳酸钠是由金属离子和酸根离子组成的化合物,属于盐类物质,其水溶液显碱性;碳酸钠与氢氧化钙反应生成氢氧化钠和碳酸钙,反应的化学方程式:![]() ;
;
(2)碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,现象A是有气泡产生,则甲溶液是碳酸钠,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,该反应由两种化合物互相交换成分,生成另外两种化合物的反应,属于基本反应类型中的复分解反应;
(3)稀盐酸与氢氧化钙反应生成氯化钙和水,步骤①乙溶液中溶质一定有氯化钙,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,②底部有白色沉淀,说明步骤①中碳酸钠有剩余,根据步骤③实验现象则上层溶液中一定含有的溶质是氯化钠,可能含有的溶质是氯化钙。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目