题目内容
(2013?宜兴市一模)高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
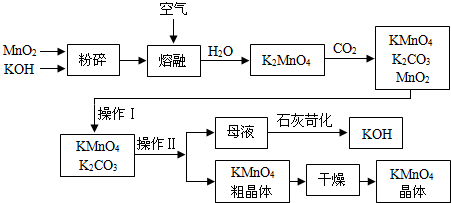
请回答下列问题:
(1)操作I的名称是
(2)请完成该工艺中生成KMnO4的反应方程式:
(3)上述流程中可以循环使用的物质是KOH和
(4)该生产中需要纯净的CO2气体.若要制备纯净的CO2所需试剂最好选择:
A.石灰石B.稀盐酸C.稀硫酸D.纯碱
(5)“石灰苛化”是向母液中加入熟石灰,试写出反应的化学方程式:

请回答下列问题:
(1)操作I的名称是
过滤
过滤
.(2)请完成该工艺中生成KMnO4的反应方程式:
3
3
K2MnO4+2
2
CO2=2
2
KMnO4+2
2
K2CO3+1
1
MnO2(3)上述流程中可以循环使用的物质是KOH和
MnO2
MnO2
(写化学式).(4)该生产中需要纯净的CO2气体.若要制备纯净的CO2所需试剂最好选择:
CD
CD
.A.石灰石B.稀盐酸C.稀硫酸D.纯碱
(5)“石灰苛化”是向母液中加入熟石灰,试写出反应的化学方程式:
K2CO3+Ca(OH)2═CaCO3↓+2KOH
K2CO3+Ca(OH)2═CaCO3↓+2KOH
.分析:(1)根据不溶于液体的固体和液体分离的一种方法考虑;(2)利用反应前后原子的个数不会变化配平即可;(3)循环使用的物质即是反应物与生成物中都具有的物质;(4)若要在实验室制备较纯净的CO2,不能采用盐酸因为他有挥发性.(5)根据方程式的写法考虑.
解答:解:(1)不溶于液体的固体和液体分离的一种方法是过滤;
(2)利用反应前后原子的个数不会变化配平,先配平钾原子个数,再配平其它系数即可解决.方程式为:3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2;
(3)循环使用的物质即是反应物与生成物中都具有的物质,反应物与生成物中均含有氢氧化钾与二氧化锰,是循环使用的物质;
(4)若要在实验室制备较纯净的CO2,不能采用盐酸因为他有挥发性,因为硫酸与碳酸钙制取二氧化碳不可取所以选择碳酸钠与硫酸;
(5)反应物是碳酸钾和氢氧化钙写在等号的左边,生成物是碳酸钙和氢氧化钾,写在等号的右边,用观察法配平即可,碳酸钙后面标上沉淀符号,所以方程式是:K2CO3+Ca(OH)2═CaCO3↓+2KOH;
故答案为:(1)过滤;(2)3;2;2;2;1;(3)MnO2;(4)CD;(5)K2CO3+Ca(OH)2═CaCO3↓+2KOH.
(2)利用反应前后原子的个数不会变化配平,先配平钾原子个数,再配平其它系数即可解决.方程式为:3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2;
(3)循环使用的物质即是反应物与生成物中都具有的物质,反应物与生成物中均含有氢氧化钾与二氧化锰,是循环使用的物质;
(4)若要在实验室制备较纯净的CO2,不能采用盐酸因为他有挥发性,因为硫酸与碳酸钙制取二氧化碳不可取所以选择碳酸钠与硫酸;
(5)反应物是碳酸钾和氢氧化钙写在等号的左边,生成物是碳酸钙和氢氧化钾,写在等号的右边,用观察法配平即可,碳酸钙后面标上沉淀符号,所以方程式是:K2CO3+Ca(OH)2═CaCO3↓+2KOH;
故答案为:(1)过滤;(2)3;2;2;2;1;(3)MnO2;(4)CD;(5)K2CO3+Ca(OH)2═CaCO3↓+2KOH.
点评:解答本题时要充分理解图中提供的信息,只有理解了图中信息才能对问题做出正确的判断

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目

 (2013?宜兴市一模)生活中处处有化学.
(2013?宜兴市一模)生活中处处有化学.