题目内容
【题目】下面是测量空气中氧气体积含量的实验:
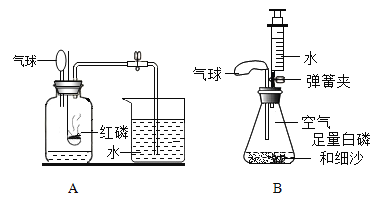
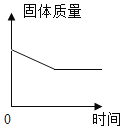
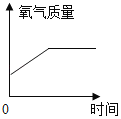
Ⅰ.实验小组按A装置进行实验,事先在集气瓶中装水的原因_____(任写一点);其所加气球的作用是_____;在整个实验过程中,可观察到气球的变化_____;实验结束后,发现进入集气瓶中水的体积超过总体积的1/5,你认为导致这一结果的原因可能是_____
A 实验前未将橡胶管夹紧 B 实验前导管中未加满水 C.红磷过量
D .氧气为消耗完 E .点燃的红磷伸入集气瓶速度过慢,使空气膨胀逸出
Ⅱ.实验A测得结果不够准确,实验小组进行反思。该小组通过查阅资料,选定白磷(与红磷一样是一种磷的单质,燃烧产物也相同)在如图B所示装置中测量空气中氧气体积分数并取得成功。
[查阅资料]白磷着火燃烧的温度为40℃。
[提出问题]氧气体积约占空气总体积的多少?
[实验准备]锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
[实验探究]装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
[现象分析]
(1)将锥形瓶底部放入热水中,目的是_____,足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体_____燃烧(填“支持”或“不支持”),瓶内剩余气体_____的氮气(填“纯净”或“不纯净”)。
(2)写出白磷在空气中燃烧的符号表达式:_____。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:
①注射器中的水自动喷射出来,导致这个现象发生的原因是:_____;
②当注射器中的水还剩约_____mL时停止下流,导致这个现象发生的原因是:_____。
(4)在实验室中白磷应保存在_____,原因是_____
【答案】降低温度或吸收五氧化二磷 缓冲作用 气球先涨大后缩小 AE 提供温度,引燃白磷 不支持 不纯净 P+O2![]() P2O5 白磷燃烧耗尽了瓶中的氧气,瓶内氧压强减小 2.5mL 红磷燃烧耗掉氧气,耗掉多少毫升的氧气,就有多少毫升的水来填充 水或者煤油中 水可以使白磷隔绝氧气
P2O5 白磷燃烧耗尽了瓶中的氧气,瓶内氧压强减小 2.5mL 红磷燃烧耗掉氧气,耗掉多少毫升的氧气,就有多少毫升的水来填充 水或者煤油中 水可以使白磷隔绝氧气
【解析】
Ⅰ.实验小组按A装置进行实验,事先在集气瓶中装水的原因是为了降低温度或吸收五氧化二磷。红磷燃烧时,瓶内气压增加,可能导致瓶塞被冲开,故加装气球可以起缓冲作用。红磷燃烧,放出热量,气体受热膨胀,内压增加,气球涨大,当反应结束温度冷却后,红磷燃烧耗尽瓶中的氧气,故气压降低,故气球缩小。A 实验前未将橡胶管夹紧,瓶内温度升高后,瓶中的气体受热膨胀,部分气体外溢,故测量结果偏大,故正确; B 实验前导管中未加满水,也会使测量结果偏小,故错误; C.该实验要求红磷必须过量,故错误;D .氧气未消耗完会使测量结果偏小,故错误; E .点燃的红磷伸入集气瓶速度过慢,使空气膨胀逸出,测量结果偏大,故正确。故选AE。
Ⅱ[现象分析]
(1)将锥形瓶底部放入热水中,目的是提供温度,引燃白磷。足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体不支持燃烧。剩余的气体中主要是氮气,还有其他的少量气体,故不是纯净的氮气。
(2)白磷与空气中的氧气点燃反应生成五氧化二磷,反应的符号表达式为:P+O2![]() P2O5
P2O5
(3)①白磷燃烧耗尽了瓶中的氧气,瓶内氧压强减小,故针筒中的水会自动射出。
②空气体积为230mL,其中氧气的体积为230mL×![]() =47.5mL,故针筒中的水剩余2.5mL。原因是红磷燃烧耗掉氧气,耗掉多少毫升的氧气,就有多少毫升的水来填充。
=47.5mL,故针筒中的水剩余2.5mL。原因是红磷燃烧耗掉氧气,耗掉多少毫升的氧气,就有多少毫升的水来填充。
(4)白磷应该保存在水或者煤油中,因为水可以使白磷隔绝氧气。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】酸、碱、盐在生产、生活中具有广泛的用途。
(1)化学实验室有失去标签的稀硫酸、氢氧化钠、酚酞、碳酸钠、硝酸钡等五瓶无色溶液,现将其任意编号:![]() ,然后两两组合进行实验,其部分现象如下表:
,然后两两组合进行实验,其部分现象如下表:
实验 |
|
|
|
|
现象 | 产生气体 | 产生沉淀 | 产生沉淀 | 溶液变红 |
①写出溶液![]() 中溶质的化学式:
中溶质的化学式:![]() _____,
_____,![]() _____。
_____。
②写出溶液![]() 与
与![]() 反应的化学方程式_____。
反应的化学方程式_____。
(2)将氯化钠和氯化钙的混合物![]() 溶于水,再加入
溶于水,再加入![]() 溶质质量分数为
溶质质量分数为![]() 的碳酸钠溶液,恰好完全反应,则该混合物中氯元素的质量分数为_____(结果精确到
的碳酸钠溶液,恰好完全反应,则该混合物中氯元素的质量分数为_____(结果精确到![]() )。
)。