题目内容
100g4%的氢氧化钠溶液与200g稀硫酸充分反应,滴入紫色石蕊试液,溶液显紫色,求:
(1)稀硫酸溶液中溶质的质量分数.
(2)反应后溶液中溶质的质量分数.
(1)稀硫酸溶液中溶质的质量分数.
(2)反应后溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:氢氧化钠溶液与稀硫酸充分反应,滴入紫色石蕊试液,溶液显紫色,说明两种物质恰好完全反应;
根据氢氧化钠溶液质量、溶质质量分数可以计算稀硫酸中硫酸的质量和生成的硫酸钠的质量,进一步可以计算稀硫酸溶液中溶质的质量分数和反应后溶液中溶质的质量分数.
根据氢氧化钠溶液质量、溶质质量分数可以计算稀硫酸中硫酸的质量和生成的硫酸钠的质量,进一步可以计算稀硫酸溶液中溶质的质量分数和反应后溶液中溶质的质量分数.
解答:解:(1)设稀硫酸中硫酸的质量为x,反应生成硫酸钠的质量为y,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98 142
100g×4% x y
=
=
,
x=4.9g,y=7.1g,
稀硫酸溶液中溶质的质量分数为:
×100%=2.45%,
答:稀硫酸溶液中溶质的质量分数为2.45%.
(2)反应后溶液中溶质的质量分数为:
×100%=2.4%,
答:反应后溶液中溶质的质量分数为2.4%.
2NaOH+H2SO4═Na2SO4+2H2O,
80 98 142
100g×4% x y
| 80 |
| 100g×4% |
| 98 |
| x |
| 142 |
| y |
x=4.9g,y=7.1g,
稀硫酸溶液中溶质的质量分数为:
| 4.9g |
| 200g |
答:稀硫酸溶液中溶质的质量分数为2.45%.
(2)反应后溶液中溶质的质量分数为:
| 7.1g |
| 100g+200g |
答:反应后溶液中溶质的质量分数为2.4%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
日常生活中的下列变化,属于物理变化的是( )
| A、酒精挥发 | B、纸张燃烧 |
| C、塑料降解 | D、百炼成钢 |
纳米碳管是一种由碳原子构成的直径为几个纳米的空心管.下列有关纳米碳管的说法错误的是( )
| A、纳米碳管是一种新型的化合物 |
| B、纳米碳管在常温下化学性质稳定 |
| C、纳米碳管管道多,吸附能力强 |
| D、纳米碳管完全燃烧后生成物是二氧化碳 |
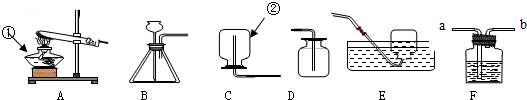
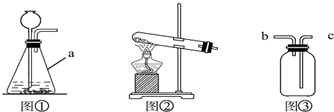
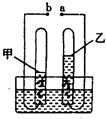 如图是通电分解水的简易装置图,回答下列问题.
如图是通电分解水的简易装置图,回答下列问题.